题目内容
13.下列离子方程式正确的是( )| A. | 以石墨作电极电解氯化镁溶液:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑ | |
| B. | 澄清石灰水与少量小苏打溶液混合:Ca2++OH-+HCO3-═CaCO3↓+H2O | |
| C. | 氯气通入蒸馏水中 Cl2+H2O═Cl-+ClO-+2 H+ | |
| D. | 次氯酸钠溶液中通入SO2气体:2ClO-+SO2+H2O═2HClO+SO32- |
分析 A.生成氢氧化镁沉淀;
B.澄清石灰水与少量小苏打溶液混合,小苏打完全反应,生成碳酸钙、NaOH、水;
C.HClO是弱酸,用化学式;
D.次氯酸根离子具有强的氧化性能够氧化亚硫酸根离子.
解答 解:A.用石墨作电极电解氯化镁溶液,离子方程式为Mg2++2Cl-+2H2O $\frac{\underline{\;电解\;}}{\;}$Mg(OH)2↓+H2↑+Cl2↑,故A错误;
B.澄清石灰水与少量小苏打溶液混合的离子反应为HCO3-+Ca2++OH-═CaCO3↓+H2O,故B正确;
C.氯气通入蒸馏水中方程式为Cl2+H2O?H++Cl-+HClO,故C错误;
D.次氯酸钠溶液中通入少量SO2气体:SO2+3ClO-+H2O=SO42-+2HClO+Cl-,故D错误.
故选B.
点评 本题考查了离子方程式的书写,为高考频考点,题目难度不大,熟悉反应的实质是解题关键,注意化学式的拆分、反应物用量对化学反应的影响.

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
13.如图所示的装置中,能够组成原电池,产生电流的是( )
| A. | 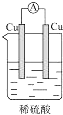 | B. | 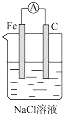 | C. | 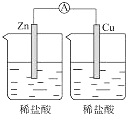 | D. | 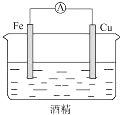 |
8.社会、生活中碰到的某些问题常常涉及到化学知识,下列说法中不正确的是( )
| A. | 全球禁用氟里昂是为了保护臭氧层不被破坏 | |
| B. | 误食重金属盐,可用喝牛奶或生鸡蛋清进行解毒 | |
| C. | 苯酚有毒,但它的稀溶液可直接用作防腐剂和消毒剂 | |
| D. | 变质的花生油有难闻的特殊气味,是由于油脂发生了水解反应 |
18.下列有关碱金属铷(Rb)的叙述中,错误的是( )
| A. | 灼烧硝酸铷时,火焰有特殊颜色 | |
| B. | 氯化铷是离子化合物 | |
| C. | 在钠、钾、铷三种单质中,铷的熔点最高 | |
| D. | 氢氧化铷是弱碱 |
5.某有机物A 是农药生产中的一种中间体,其结构简式如图,下列叙述中正确的是( )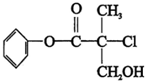

| A. | 有机物A 属于芳香烃 | |
| B. | 有机物A 可以与Br2的CCl4溶液发生加成反应 | |
| C. | 有机物A 与浓硫酸混合加热,可以发生消去反应 | |
| D. | 有机物A 可与NaOH 溶液反应,生成多种可溶于水的化合物 |
2.向某溶液中加入含Fe2+的溶液后,无明显变化.当再滴入几滴新制氯水后,混合溶液变成红色,则下列结论错误的是( )
| A. | 该溶液中一定含有SCN- | B. | 氧化性:Fe2+>Cl2 | ||
| C. | Fe2+与SCN-不能形成红色物质 | D. | Fe2+被氧化为Fe3+ |
3.下列说法正确的是( )
| A. | 侯德榜提出的联合制碱法可大大提高氯化钠的利用率 | |
| B. | 具有永久硬度的硬水可以采用加热的方法进行软化 | |
| C. | CO.CH4、CH3OH是一碳化学的主要原料 | |
| D. | 复合材料一般由起黏结作用的基体和起增强作用的增强体构成 | |
| E. | 油脂和氢氧化钠共热产生的混合物,加入食盐可使肥皂析出. |
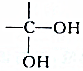 结构的有机物不能稳定存在,根据以上信息,试回答:
结构的有机物不能稳定存在,根据以上信息,试回答: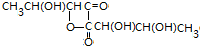 +2H2O,是酯化反应.
+2H2O,是酯化反应.