��Ŀ����
����Ŀ�� ����ͨ������
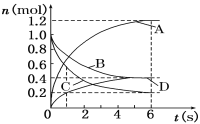
ij�¶�ʱ����һ��2L���ܱ������У�X��Y��Z�����������ʵ����ʵ�����ʱ��ı仯������ͼ��ʾ������ͼ�����ݣ�����д���пհף�

��1���÷�Ӧ�Ļ�ѧ����ʽΪ ��
��2���ӿ�ʼ��2min��Z��ƽ����Ӧ����Ϊ ��
ƽ��ʱ��X��ת����Ϊ ��ƽ��ʱ��Y��Ũ��Ϊ ��
��3������������˵���÷�Ӧ�Ѵﵽ��ѧƽ��״̬���ǣ����ţ� ��
A������ѹǿ���ٷ����仯
B X������������ٷ����仯
C����������ԭ���������ٷ����仯
D��ͬʱ��������2n mol��Z��ͬʱ����n mol��Y
E�� ��ͬʱ��������n mol��Y��ͬʱ����3n mol��X
���𰸡�18����1��3X+Y2Z ��2��0��05molL-1min-1 30% 4��5mol/L ��3��ABD
��������
�����������1����n��X��=0��3mol����n��Y��=0��1mol����n��Z��=0��2mol��������������֮��Ϊ3��1��2���÷�Ӧ�Ļ�ѧ����ʽΪΪ��3X+Y2Z����2��v��Z��=��C/��t=0��2/2x2=0��05molL-1min-1���ӿ�ʼ��2min��Z��ƽ����Ӧ����ΪΪ��0��05molL-1min-1��Xת�������ʵ���Ϊ1��0mol-0��7mol=0��3mol��ת����Ϊ0��3/1��0��100%=30%������ͼ���п�֪��ƽ��ʱ��Y��Ũ��Ϊ0��9/2=4��5mol/L��3����Ӧǰ���������ʵ�����ͬ����ѹǿ����ʱ����������ʵ������䣬�ﵽ��ѧƽ��״̬��A��ȷ����������ʵ����������ʹX������������ٷ����仯���ﵽ��ѧƽ��״̬��B��ȷ������ԭ���غ㶨�ɣ�����ƽ���������������ԭ�����������ᷢ���仯��C������ͬʱ��������2n mol��Z��ͬʱ����n mol��Y��������˵��V������=V���棩��D��ȷ����ͬʱ��������n mol��Y��ͬʱ����3n mol��X��������˵��V������=V��������E��������������˵���÷�Ӧ�Ѵﵽ��ѧƽ��״̬����ABD��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ���Ȼ�ͭ����(CuCl2��2H2O)�к���FeCl2���ʣ�Ϊ�Ƶô������Ȼ�ͭ���壬���Ƚ����Ƴ�ˮ��Һ���ٰ���ͼ��ʾ�IJ�����������ᴿ��

������±�������������ա�
�������↑ʼ����ʱ��pH | �������������ȫʱ��pH | |
Cu2�� | 4.7 | 6.7 |
Fe2�� | 7.0 | 9.0 |
Fe3�� | 1.9 | 3.7 |
(1)����I����X��Ŀ����_________________��
(2)�������ʶ�������ΪX���ʺϱ�ʵ���X���ʿ�����(��ѡ��)_________ ��
A��KMnO4 B��NaClO C��H2O2 D��Cl2
(3)����II��Y�Լ�Ϊ____________(�ѧʽ)����������Һ��pH��______��Χ��
(4)ʵ����������CuCl2��Һʱ���������_________(����������)��������(�������������й����ӷ���ʽ��ʾ)_________________ __________��
(5)����CuCl2��Һ�������գ��õ��Ĺ�����_________________(�ѧʽ)����Ҫ����ˮCuCl2���������������_________________________��