��Ŀ����
����Ŀ��һ���¶��£����ݻ�Ϊ2 L���ܱ�������ͨ���������巢����ѧ��Ӧ����Ӧ�и����ʵ����ʵ����仯����ͼ��ʾ���Ը÷�Ӧ���ƶϺ�������( )
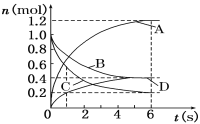
A���÷�Ӧ�Ļ�ѧ����ʽΪ3B��4D ![]() 6A��2C
6A��2C
B����Ӧ���е�1 sʱ��v(A)��v(D)
C����Ӧ���е�6 sʱ��B��ƽ����Ӧ����Ϊ0.05 mol/(L��s)
D����Ӧ���е�6 sʱ�������ʵķ�Ӧ�������
���𰸡�C
��������
���������A������ͼ��A��DΪ�����B��CΪ��Ӧ����ݻ�ѧ��Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ����A��D��B��C��ϵ��֮��1.2��0.4��(1��0.4)��(1��0. 2)=6��2��3��4����˷�Ӧ����ʽΪ3B+4C![]() 6A+2D���ʴ���B����ѧ��Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ�v(A)��v(D)=3��1���ʴ���C�����ݻ�ѧ��Ӧ���ʵĶ��壬v(B)=(1��0.4)/(2��6)mol/(L��s)=0.05 mol/(L��s)������ȷ��D����ѧ��Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ��ʴ���
6A+2D���ʴ���B����ѧ��Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ�v(A)��v(D)=3��1���ʴ���C�����ݻ�ѧ��Ӧ���ʵĶ��壬v(B)=(1��0.4)/(2��6)mol/(L��s)=0.05 mol/(L��s)������ȷ��D����ѧ��Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ��ʴ���

��ϰ��ϵ�д�
�����Ŀ