题目内容
2.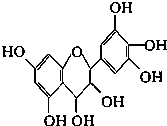 从葡萄籽中提取的原花青素结构为:原花青素具有生物活性,如抗氧化和自由基清除能力等,可防止机体内脂质氧化和自由基的产生而引发的肿瘤等多种疾病.有关原花青素的下列说法不正确的是( )
从葡萄籽中提取的原花青素结构为:原花青素具有生物活性,如抗氧化和自由基清除能力等,可防止机体内脂质氧化和自由基的产生而引发的肿瘤等多种疾病.有关原花青素的下列说法不正确的是( )| A. | 该物质既可看作醇类,也可看作酚类 | |
| B. | 1mol该物质可与4molBr2反应 | |
| C. | 1mol该物质可与7molNaOH反应 | |
| D. | 1mol该物质可与7molNa反应 |
分析 分子中含有酚羟基,可发生取代、氧化和显色反应,含有醇羟基,可发生取代、氧化和消去反应,以此解答该题.
解答 解:A.分子中含有酚羟基和醇羟基,可看作醇类,也可看作酚类,故A正确;
B.分子中含有2个苯环,5个酚羟基,共有4个H原子可被取代,故B正确;
C.分子中只有酚羟基与氢氧化钠反应,则1 mol该物质可与5 mol NaOH反应,故C错误;
D.分子中共含有7个羟基,则1 mol该物质可与7 mol Na反应,故D正确.
故选C.
点评 本题考查有机物的结构与性质,为高考常见题型,把握有机物中的官能团为解答本题的关键,熟悉醇、酚的性质即可解答,题目难度不大.

练习册系列答案
相关题目
14.下列物质中含离子键的是( )
| A. | HCl | B. | CH4 | C. | NaH | D. | NH3 |
15.异丙基环己烷[ -CH(CH3)2]分子的一氯取代物的同分异构体的数目有( )
-CH(CH3)2]分子的一氯取代物的同分异构体的数目有( )
 -CH(CH3)2]分子的一氯取代物的同分异构体的数目有( )
-CH(CH3)2]分子的一氯取代物的同分异构体的数目有( )| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
17.在元素周期表的第四周期的主族元素中,金属元素的种数是( )
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
14.下列有关物质的应用或性质的说法正确的是( )
| A. | 运用水玻璃堵塞管道,是因为水玻璃显碱性 | |
| B. | 配制碘水时,常加入少量的KI,目的是防止I2被还原 | |
| C. | 用酸化的高锰酸钾与H2O2可制取少量氧气,KMnO4作催化剂 | |
| D. | 明矾[KAl(SO4)2•12H2O]净水和液氯(Cl2)净水的原理不相同 |
11.苯甲酸广泛用于制药和化工行业,某同学尝试用甲苯的氧化反应制备苯甲酸,反应原理:

实验方法:一定量的甲苯和KMnO4溶液在100℃反应一段时间后停止反应,按如下流程分离出苯甲酸和回收未反应的甲苯.
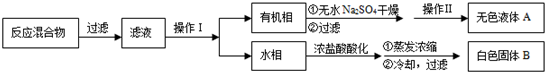
已知:苯甲酸分子量122,熔点122.4℃,在25℃和95℃时溶解度分别为0.3g和6.9g;纯净固体有机物都有固定熔点.
(1)操作Ⅰ为分液,操作Ⅱ为蒸馏.
(2)无色液体A是甲苯,定性检验A的试剂是酸性KMnO4溶液,现象是紫色溶液褪色.
(3)测定白色固体B的熔点,发现其在115℃开始熔化,达到130℃时仍有少量不熔,该同学推测白色固体B是苯甲酸与KCl的混合物,设计了如下方案进行提纯和检验,实验结果表明推测正确.请在答题卡上完成表中内容.
(4)纯度测定:称取1.220g产品,配成100ml甲醇溶液,移取25.00ml溶液,滴定,消耗KOH的物质的量为2.40×10-3mol,产品中苯甲酸质量分数的计算表达为$\frac{2.4×10{\;}^{-3}mol×4×122g/mol}{1.22g}$,计算结果为96%(保留二位有效数字).

实验方法:一定量的甲苯和KMnO4溶液在100℃反应一段时间后停止反应,按如下流程分离出苯甲酸和回收未反应的甲苯.

已知:苯甲酸分子量122,熔点122.4℃,在25℃和95℃时溶解度分别为0.3g和6.9g;纯净固体有机物都有固定熔点.
(1)操作Ⅰ为分液,操作Ⅱ为蒸馏.
(2)无色液体A是甲苯,定性检验A的试剂是酸性KMnO4溶液,现象是紫色溶液褪色.
(3)测定白色固体B的熔点,发现其在115℃开始熔化,达到130℃时仍有少量不熔,该同学推测白色固体B是苯甲酸与KCl的混合物,设计了如下方案进行提纯和检验,实验结果表明推测正确.请在答题卡上完成表中内容.
| 序号 | 实验方案 | 实验现象 | 结论 |
| ① | 将白色固体B加入水中,加热溶解, 冷却、过滤 | 得到白色晶体和无色溶液 | |
| ② | 取少量滤液于试管中,滴入适量的硝酸酸化的AgNO3溶液 | 生成白色沉淀 | 滤液含Cl- |
| ③ | 干燥白色晶体,加热使其熔化,测其熔点 | 熔点为122.4℃ | 白色晶体是苯甲酸 |
12.除去如表各组物质中的少量杂质,所用方法正确的是( )
| 选项 | 物质 | 杂质 | 除杂方法 |
| A | Cu | CuO | 在空气中灼烧 |
| B | CaO | Ca(OH)2 | 加入足量的稀盐酸 |
| C | H2 | CO | 通入O2,点燃 |
| D | O2 | H2O | 通过浓硫酸洗气 |
| A. | A | B. | B | C. | C | D. | D |
 ).
).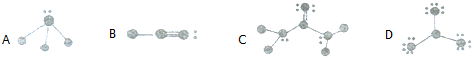
 、
、 .
.