题目内容
11.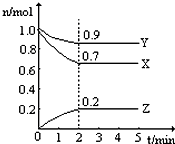 某温度时,在一个2L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白:
某温度时,在一个2L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白:(1)该反应的化学方程式为3X+Y?2Z;
(2)从开始至2min,Z的平均反应速率为0.05mol/(L.min);
(3)反应达平衡时:体系的压强是开始的0.9倍;
(4)X的转化率=30%.(转化率为反应掉的物质的量除以原来的物质的量).
分析 根据图象知,随着反应进行,X、Y的物质的量减少而Z物质的量增大,说明X、Y是反应物而Z是生成物,
(1)达到平衡状态时,参加反应的△n(X)=(1.0-0.7)mol=0.3mol、△n(Y)=(1.0-0.9)mol=0.1mol、△n(Z)=(0.2-0)mol=0.2mol,同一反应中同一时间段内参加反应的各物质的物质的量之比等于其计量数之比,所以X、Y、Z的计量数之比=0.3mol:0.1mol:0.2mol=3:1:2,据此书写方程式;
(2)Z的平均反应速率=$\frac{\frac{△n}{V}}{△t}$;
(3)恒温恒容条件下,气体的物质的量之比等于其压强之比;
(4)X的转化率=$\frac{转化量}{起始量}$×100%计算.
解答 解:根据图象知,随着反应进行,X、Y的物质的量减少而Z物质的量增大,说明X、Y是反应物而Z是生成物,
(1)达到平衡状态时,参加反应的△n(X)=(1.0-0.7)mol=0.3mol、△n(Y)=(1.0-0.9)mol=0.1mol、△n(Z)=(0.2-0)mol=0.2mol,同一反应中同一时间段内参加反应的各物质的物质的量之比等于其计量数之比,所以X、Y、Z的计量数之比=0.3mol:0.1mol:0.2mol=3:1:2,所以该反应方程式为3X+Y?2Z,
故答案为:3X+Y?2Z;
(2)Z的平均反应速率=$\frac{\frac{△n}{V}}{△t}$=$\frac{\frac{0.2}{2}}{2}$=0.05mol/(L.min),故答案为:0.05mol/(L.min);
(3)根据图象知,未反应时混合气体的物质的量=(1.0+1.0)mol=2.0mol,平衡状态混合气体物质的量=(0.9+0.7+0.2)mol=1.8mol,恒温恒容条件下,气体的物质的量之比等于其压强之比,所以平衡状态体系压强是开始时的$\frac{1.8mol}{2.0mol}$=0.9倍,
故答案为:0.9;
(4)X的转化率=$\frac{转化量}{起始量}$×100%=$\frac{1-0.7}{1}$×100%=30%,故答案为:30%.
点评 本题考查图象分析,侧重考查学生分析及计算能力,明确曲线变化趋势含义、物质的量变化量与其计量数的关系即可解答,难点是(3)题计算,题目难度中等.

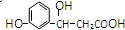 ,它不可以发生的反应类型有:①加成;②水解;③消去;④酯化;⑤银镜;⑥氧化;⑦取代;⑧加聚;⑨缩聚.( )
,它不可以发生的反应类型有:①加成;②水解;③消去;④酯化;⑤银镜;⑥氧化;⑦取代;⑧加聚;⑨缩聚.( )| A. | ①⑤⑧ | B. | ①②⑤⑨ | C. | ②⑥⑧⑨ | D. | ②⑤⑧ |
| 实验方案 | 实验现象 |
| ①用砂纸摩擦后的镁带与沸水反应,再向反应 应后溶液中滴加酚酞 | A、浮于水面,熔成一个小球,在水面上无定向移 动,随之消失,溶液变红色 |
| ②钠与滴有酚酞试液的冷水反应 | B、产生气体,可在空气中燃烧,溶液变成浅红色 |
| ③镁条与2mol•L-1的盐酸反应 | C、反应不十分强烈,产生无色气体 |
| ④铝条与2mol•L-1的盐酸反应 | D、剧烈反应,产生无色气体 |
| ⑤向AlCl3溶液中滴加NaOH溶液至过量 | E、生成白色胶状沉淀,继而沉淀消失 |
(1)实验目的验证第三周期金属元素的金属性的递变规律.
(2)实验用品:
仪器:试管、酒精灯、砂纸、镊子、小刀、胶头滴管、滤纸
药品:镁带、钠、铝条、2mol•L-1的盐酸、NaOH溶液、蒸馏水、酚酞、AlCl3溶液
(3)实验内容:(填写题给信息表中的序号)
| 实验方案 | 实验现象(填写序号) |
| ① | B |
| ② | A |
| ③ | D |
| ④ | C |
| ⑤ | E |
(5)为了用实验的方法验证镁和铝的金属性强弱,学生乙设计了一种不同于学生甲的方法:
学生甲:用2mol•L-1盐酸作试剂,比较镁和铝与盐酸反应的情况
学生乙:用水作试剂,比较镁和铝与水反应的情况
试判断学生乙的设计方案是否合理不合理,原因是常温下镁和铝几乎不和水发生反应,而和酸反应较明显.
| A. | NaAlO2溶液中通入过量的CO2:2AlO2-+3H2O+CO2═2Al(OH)3↓+CO32- | |
| B. | 明矾溶液中滴加Ba(OH)2溶液至SO42-完全沉淀:Al3++Ba2++SO42-+3OH-═BaSO4↓+Al(OH)3↓ | |
| C. | 200 mL 2 mol/L的FeBr2溶液中通入11.2 L标准状况下的氯气:4Fe2++6Br-+5Cl2═4Fe3++3Br2+10Cl- | |
| D. | 在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO-+2Fe(OH)3═2FeO42-+3Cl-+H2O+4H+ |
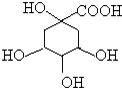 奎尼酸是制备艾滋病新药二咖啡酰奎尼酸的原料,其结构简式如图,下列有关奎尼酸的说法中正确的是( )
奎尼酸是制备艾滋病新药二咖啡酰奎尼酸的原料,其结构简式如图,下列有关奎尼酸的说法中正确的是( )| A. | 奎尼酸的分子式是C7H9O6 | |
| B. | 1mol奎尼酸与足量NaOH溶液反应,最多消耗NaOH物质的量为5mol | |
| C. | 1 mol奎尼酸与足量钠反应生成56L氢气 | |
| D. | 奎尼酸能发生消去反应,也能与乙醇、乙酸发生取代反应 |
| A. | Li的熔点高于Na的熔点 | |
| B. | CaF2晶体中Ca2+的配位数为4 | |
| C. | 干冰晶体中每个CO2分子周围距离相等且最近的CO2分子数为10个 | |
| D. | SiO2 的晶体中最小环上的原子个数为6个 |
| A. | 4 g氦气中含有的分子数和原子数均为NA | |
| B. | 标准状况下,22.4 L CCl4中含有的分子数为NA | |
| C. | 1 L 0.1 mol•L-1乙醇溶液中含有的氧原子数为0.1NA | |
| D. | 1 mol Cl2完全反应转移的电子数一定是2NA |
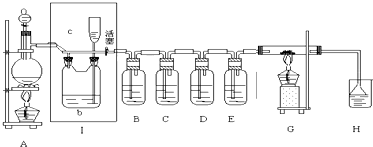
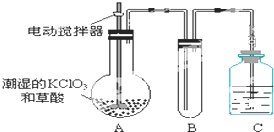 用二氧化氯(ClO2)、铁酸钠(Na2FeO4摩尔质量为166g•mol-1)等新型净水剂替代传统的净水剂Cl2对淡水进行消毒是城市饮用水处理新技术.ClO2和Na2FeO4在水处理过程中分别被还原为Cl-和Fe3+.
用二氧化氯(ClO2)、铁酸钠(Na2FeO4摩尔质量为166g•mol-1)等新型净水剂替代传统的净水剂Cl2对淡水进行消毒是城市饮用水处理新技术.ClO2和Na2FeO4在水处理过程中分别被还原为Cl-和Fe3+.