题目内容
18.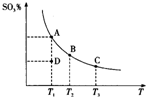 二氧化硫的催化氧化原理为2SO2(g)+O2(g)?2SO3(g),反应混合体系在平衡状态时SO3的百分含量与温度的关系如图所示.下列说法正确的是( )
二氧化硫的催化氧化原理为2SO2(g)+O2(g)?2SO3(g),反应混合体系在平衡状态时SO3的百分含量与温度的关系如图所示.下列说法正确的是( )| A. | 在D点时,反应逆向进行 | |
| B. | 反应2SO2(g)+O2(g)?2SO3(g)的△H>0 | |
| C. | 若B、C点的平衡常数分别为KB、KC,则KB>KC | |
| D. | 恒温恒压下向平衡体系中通入氦气,平衡向左移动 |
分析 A、D点SO3的百分含量低于相同温度平衡点的含量,说明D点未到达平衡状态,可逆反应在一定条件下进行的最终状态是平衡状态,所以反应向正反应移动;
B、曲线上的点都是平衡点,由图可知,温度越高,SO3的百分含量越低,说明升高温度平衡向逆反应移动;
C、升高温度,平衡向逆反应移动,故温度越高平衡常数越小;
D、恒温恒压下向平衡体系中通入氦气,体积增大,压强降低,平衡向体积增大的方向移动.
解答 解:A、曲线上的点都是平衡点,D点SO3的百分含量低于相同温度平衡点的含量,说明D点未到达平衡状态,反应向正反应移动,故A错误;
B、曲线上的点都是平衡点,由图可知,温度越高,SO3的百分含量越低,说明升高温度平衡向逆反应移动,故该反应正反应是放热反应,则△H<0,故B错误;
C、升高温度,平衡向逆反应移动,故温度越高平衡常数越小,B点的温度低于C的温度,故平衡常数,KB>KC,故C正确;
D、恒温恒压下向平衡体系中通入氦气,体积增大,参与反应气体压强降低,平衡向体积增大的方向移动,即向平衡向左移动,故D正确.
故选CD.
点评 本题考查化学平衡图象、化学平衡移动的影响因素等,难度中等,注意根据SO3的含量判断平衡移动的方向.

练习册系列答案
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案
相关题目
12.25℃时,NH3•H2O和CH3COOH的电离常数K相等.下列说法正确的是( )
| A. | 常温下,CH3COONH4溶液的pH=7,与纯水中H2O的电离程度相同 | |
| B. | 向CH3COONH4溶液加入CH3COONa固体时,c(NH4+)、c(CH3COO-)均会增大 | |
| C. | 常温下,等浓度的NH4Cl和CH3COONa两溶液的pH之和为14 | |
| D. | 等温等浓度的氨水和醋酸两溶液加水稀释到相同体积,溶液pH的变化值一定相同 |
6.HA为酸性略强于醋酸的一元弱酸,则下列叙述正确的是( )
| A. | 0.1mol•L-1 HA 中c(H+)=c(OH-)+c(A-), | |
| B. | 0.1mol•L-1 HA 与 0.1 mol•L-1NaOH 混合至溶液呈中性:c(Na+)<c(A-) | |
| C. | 0.1mol•L-1 NaA 中c(Na+)>c(OH-)>c(A-)>c(H+) | |
| D. | 0.1mol•L-1 HA中加入少量NaA固体,HA的电离常数减小 |
13.分某学习小组在研究水处理问题时,将一定量NaClO溶液与FeSO4溶液相混合,得到含有大量悬浮物的混合液.请完成对反应物剩余情况的探究.
(1)提出合理假设:
假设1:FeSO4有剩余;
假设2:NaClO有剩余;
假设3:NaClO和FeSO4都无剩余
(2)样品初步处理:取少量混合液于试管中,滴加足量稀硫酸得到澄清溶液.此澄清溶液中肯定含有的金属阳离子是Na+,Fe3+
(3)设计后续实验方案验证假设.请在答题卡上写出实验步骤以及预期现象和结论.限选实验试剂:3mol.L-1 H2SO4,0.01mol•L-1 KMnO4,20% KSCN、3% H2O2,淀粉-KI溶液、紫色石蕊溶液.
(1)提出合理假设:
假设1:FeSO4有剩余;
假设2:NaClO有剩余;
假设3:NaClO和FeSO4都无剩余
(2)样品初步处理:取少量混合液于试管中,滴加足量稀硫酸得到澄清溶液.此澄清溶液中肯定含有的金属阳离子是Na+,Fe3+
| 实验步骤 | 预期现象和结论 | |
| 步骤1 | 将上述澄清溶液分置于A、B试管中. | |
| 步骤2 | ||
| 步骤3 | ||
10.已知:将C12通入适量NaOH溶液,产物中可能有NaCl、NaClO、NaClO3,且$\frac{c(C{l}^{-})}{c(Cl{O}^{-})}$的值仅与温度高低有关.当n(NaOH)=6amol时,下列有关说法正确的是( )
| A. | 改变温度,反应中转移电子的物质的量n的范围:3amol≤n≤5amol | |
| B. | 改变温度,产物中NaCl的最小理论产量为4amol | |
| C. | 参加反应的氯气的物质的量3amol | |
| D. | 某温度下,若反应后$\frac{c(C{l}^{-})}{c(Cl{O}^{-})}$=6,则溶液中$\frac{c(C{l}^{-})}{c(C{O}_{3}^{-})}=\frac{1}{2}$ |
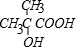 ;b 的结构简式
;b 的结构简式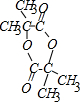 .
.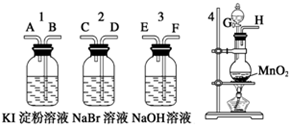 为了比较卤素单质的氧化性强弱,可在实验室先制取Cl2,并将Cl2依次通入NaBr溶液和淀粉KI溶液中.有如图所示的仪器(橡胶塞均为双孔)及药品,试回答:
为了比较卤素单质的氧化性强弱,可在实验室先制取Cl2,并将Cl2依次通入NaBr溶液和淀粉KI溶液中.有如图所示的仪器(橡胶塞均为双孔)及药品,试回答: .
.