��Ŀ����
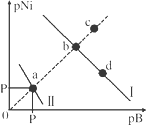
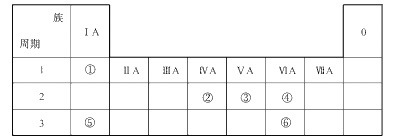
����Ŀ��Q��X��Y��ZΪ������Ԫ�أ����������ڱ��е�λ����ͼ��ʾ��
X | Y | ||
Q | Z |
��4��Ԫ�ص�ԭ������������֮��Ϊ22���ݴ˻ش��������⣺
(1)Q�ĵ��ʳ����������뵼�壬��Q��Ԫ�����ڱ��е�λ��Ϊ________��
(2)X����ͼ��⻯��ĽṹʽΪ__________��
(3)Q��X��Z����ۺ������У�������ǿ����____________��
(4)X��Y����3��Ԫ���γɵĻ������мȺ������Ӽ��ֺ��й��ۼ�����________(��дһ�ֵĻ�ѧʽ)��
(5)X�ļ��⻯����Y�ĵ����ڴ����������·�Ӧ��������������÷�Ӧ�Ļ�ѧ����ʽΪ_______��
���𰸡� �����ڣ���A�� ![]() HClO4 NH4NO3��NH4NO2 4NH3+5O2
HClO4 NH4NO3��NH4NO2 4NH3+5O2![]() 4NO+6H2O
4NO+6H2O
������������Ԫ�������ڱ��е�λ�ÿ�֪X��Yλ�ڵڶ����ڣ�Q��Zλ�ڵ������ڡ���Q��������������n����X��Y��Z��ԭ�������������ֱ���n+1��n+2��n+3����n+n+1+n+2+n+3��22�����n��4������X��N��Y��O��Z��Cl��Q��Si�����Ԫ�������ɺ�������ʵ����ʽ��
�������Ϸ�����֪X��N��Y��O��Z��Cl��Q��Si����
(1)��ĵ��ʳ����������뵼�壬��Ԫ�ص�ԭ��������14����Ԫ�����ڱ��е�λ��Ϊ�������ڵڢ�A�塣
(2)X����ͼ��⻯���ǰ������ṹʽΪ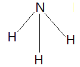 ��
��
(3)�ǽ�����Խǿ��ۺ����������Խǿ�����Q��X��Z����ۺ������У�������ǿ����HClO4��
(4)N��O��H3��Ԫ���γɵĻ������мȺ������Ӽ��ֺ��й��ۼ�����NH4NO3��NH4NO2)��
(5)X�ļ��⻯����Y�ĵ����ڴ����������·�Ӧ������������������Ĵ��������÷�Ӧ�Ļ�ѧ����ʽΪ4NH3+5O2![]() 4NO+6H2O��
4NO+6H2O��

����Ŀ����ҵ�����������������Ⱦ���������·�Ӧ��CH4��g��+2NO2��g��N2��g��+CO2��g��+2H2O��g����H=a kJ/mol ���¶�T1��T2ʱ���ֱ�0.50mol CH4��1.2mol NO2�������Ϊ1L���ܱ������У����n��CH4����ʱ��仯�������±�������˵������ȷ���ǣ�������
�¶� | ʱ��/min | 0 | 10 | 20 | 40 | 50 |
T1 | n��CH4�� | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
T2 | n��CH4�� | 0.50 | 0.30 | 0.18 | �� | 0.15 |
A.10 min�ڣ�T1ʱCH4�Ļ�ѧ��Ӧ���ʱ�T2ʱС
B.�¶ȣ�T1��T2
C.a��0
D.ƽ�ⳣ����K��T1����K��T2��