题目内容
【题目】工业上消除氮氧化物的污染,可用如下反应:CH4(g)+2NO2(g)N2(g)+CO2(g)+2H2O(g)△H=a kJ/mol 在温度T1和T2时,分别将0.50mol CH4和1.2mol NO2充入体积为1L的密闭容器中,测得n(CH4)随时间变化数据如下表:下列说法不正确的是( )
温度 | 时间/min | 0 | 10 | 20 | 40 | 50 |
T1 | n(CH4) | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
T2 | n(CH4) | 0.50 | 0.30 | 0.18 | … | 0.15 |
A.10 min内,T1时CH4的化学反应速率比T2时小
B.温度:T1<T2
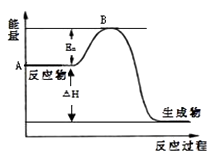
C.a<0
D.平衡常数:K(T1)<K(T2)
【答案】D
【解析】A.10 min内,T1时υ(CH4)= ![]() =0.015molL﹣1min﹣1,T2时时υ(CH4)=
=0.015molL﹣1min﹣1,T2时时υ(CH4)= ![]() =0.02molL﹣1min﹣1,T1时υ(CH4)比T2时小,故A不符合题意;
=0.02molL﹣1min﹣1,T1时υ(CH4)比T2时小,故A不符合题意;
B.温度升高,反应速率加快,因此T2>T1,故B不符合题意;
C.温度升高,甲烷剩余量增多,说明反应向左进行,正反应放热,所以a<0,故C不符合题意;
D.T1时反应进行的更为彻底,因此平衡常数更大,K(T1)>K(T2),故D符合题意;
故答案为:D.
A.根据表中数据计算不同温度下的反应速率,然后进行比较即可;
B.根据温度对化学反应速率的影响进行判断;
C.根据温度对化学平衡的影响进行判断;
D.根据温度对化学平衡的影响,判断化学平衡常数的变化即可.

【题目】Q、X、Y和Z为短周期元素,它们在周期表中的位置如图所示。
X | Y | ||
Q | Z |
这4种元素的原子最外层电子数之和为22。据此回答下列问题:
(1)Q的单质常用于制作半导体,则Q在元素周期表中的位置为________。
(2)X的最低价氢化物的结构式为__________。
(3)Q、X、Z的最高价含氧酸中,酸性最强的是____________。
(4)X、Y和氢3种元素形成的化合物中既含有离子键又含有共价键的是________(任写一种的化学式)。
(5)X的简单氢化物与Y的单质在催化加热条件下反应生成两种氧化物,该反应的化学方程式为_______。