题目内容
11.下列叙述正确的是( )| A. | 烷烃与烯烃不可能是同分异构体 | |
| B. | 同分异构体只能存在于有机化合物之间 | |
| C. | 乙酸和甲酸甲酯不互为同分异构体 | |
| D. | 乙醇、丙三醇互为同系物,同系物之间不可能互为同分异构体 |
分析 A、具有相同的分子式,结构不同的化合物互称为同分异构体,烷烃中只存在单键,烯烃中存在双键,饱和度不一样,分子式不可能相同;
B、同分异构体也可存在与无机物中;
C、乙酸与甲酸甲酯分子式相同,结构不同;
D、乙醇为饱和一元醇,丙三醇为三元醇,结构不同,不属于同系物.
解答 解:A、烷烃中只存在单键,烯烃中存在双键,饱和度不一样,分子式不可能相同,故A正确;
B、同分异构现象多存在有机物中,但同分异构体也可存在与无机物中,故B错误;
C、乙酸与甲酸甲酯分子式相同,结构不同,属于同分异构体,故C错误;
D、乙醇为饱和一元醇,丙三醇为三元醇,结构不同,不属于同系物,故D错误,
故选A.
点评 本题考查同分异构体,比较基础,注意把握同分异构体概念的内涵与外延.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.某溶液既能溶解Al(OH)3,又能溶解H2SiO3,在该溶液中可以大量共存的离子组是( )
| A. | K+、Na+、HCO3-、NO3- | B. | Ag+、K+、NO3-、Na+ | ||
| C. | H+、Mg2+、SO42-、NO3- | D. | Na+、SO42-、Cl-、ClO- |
2.在一定温度下的恒容密闭容器中,当下列物理量不再发生变化时,表明反应A(s)+3B(g)?2C(g)+D(g)已达平衡状态的是( )
①混合气体的压强 ②混合气体的密度 ③B的物质的量浓度 ④气体的总物质的量 ⑤混合气体的平均相对分子质量.
①混合气体的压强 ②混合气体的密度 ③B的物质的量浓度 ④气体的总物质的量 ⑤混合气体的平均相对分子质量.
| A. | ①②③ | B. | ②③⑤ | C. | ①③⑤ | D. | ①④⑤ |
19.常温时,1mol/L的CH3COOH溶液和0.1mol/L的CH3COOH溶液,其[H+]之比为( )
| A. | 1:1 | B. | 10:1 | C. | <10:1 | D. | >10:1 |
20.X、Y、Z、W、T是原子序数依次增大的前四个周期的元素,其中有两种是常见金属元素.其相关信息如表:
(1)X、Y、Z三种元素的电负性由大到小的顺序是O>C>Al(用元素符号表示,下同);在H-X、H-Y两种共价键中,键的极性较大的是H-O.
(2)T2+的电子排布式为1s22s22p63s23p63d6;T的单质在高温下与Y的氢化物反应,其化学方程式为3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2;工业上用W的氧化物与X的单质高温下反应制得W单质的粗产品,其化学反应方程式为SiO2+2C $\frac{\underline{\;高温\;}}{\;}$Si+2CO↑.
(3)两种氢化物X2H2和H2Y2中沸点较高的是H2O2,两者沸点相差很大的原因是H2O2分子之间存在氢键,而C2H2分子之间为范德华力.
(4)在25℃、101kPa下,已知W稳定的气态氢化物在Y的气态单质中完全燃烧,恢复至原来状态,平均每消耗4gW稳定的气态氢化物放热190.0KJ,则该反应的热化学方程式SiH4(g)+2O2(g)=SiO2(s)+2H2O(l)△H=-1520kJ/mol.
| 元素 | 相关信息 |
| X | X一种核素在考古时常用来坚定一些文物的年代 |
| Y | Y基态原子的s轨道电子与P轨道电子数相等 |
| Z | Z是所在周期的单核离子中半径最小 |
| W | W的单质被誉为“信息革命的催化剂”常用做半导体材料 |
| T | T有多种氧化物,其中一种纯净的氧化物可用来作录音磁带和 电讯器材的原材料 |
(2)T2+的电子排布式为1s22s22p63s23p63d6;T的单质在高温下与Y的氢化物反应,其化学方程式为3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2;工业上用W的氧化物与X的单质高温下反应制得W单质的粗产品,其化学反应方程式为SiO2+2C $\frac{\underline{\;高温\;}}{\;}$Si+2CO↑.
(3)两种氢化物X2H2和H2Y2中沸点较高的是H2O2,两者沸点相差很大的原因是H2O2分子之间存在氢键,而C2H2分子之间为范德华力.
(4)在25℃、101kPa下,已知W稳定的气态氢化物在Y的气态单质中完全燃烧,恢复至原来状态,平均每消耗4gW稳定的气态氢化物放热190.0KJ,则该反应的热化学方程式SiH4(g)+2O2(g)=SiO2(s)+2H2O(l)△H=-1520kJ/mol.
1.下列反应或过程需要吸收能量的是( )
| A. | H+H→H-H | B. | H-Cl→H+Cl | ||
| C. | Mg+2HCl=MgCl2+H2↑ | D. | H2SO4+2NaOH=Na2SO4+2H2O |
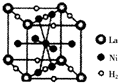 镍及其化合物在合金材料以及催化剂等方面应用广泛.
镍及其化合物在合金材料以及催化剂等方面应用广泛. ④HCHO,其中碳原子采取sp2杂化有①③④,HCHO分子内σ键与π键个数之比为3:1.
④HCHO,其中碳原子采取sp2杂化有①③④,HCHO分子内σ键与π键个数之比为3:1.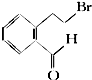 下面的框图是应用2-(2-溴乙基)苯甲醛为原料合成有机化合物C和F的流程图:
下面的框图是应用2-(2-溴乙基)苯甲醛为原料合成有机化合物C和F的流程图: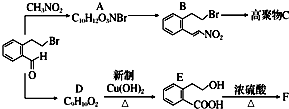
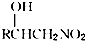
 .
.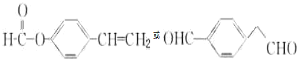 .
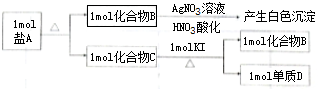
.
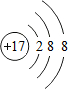 ;
;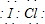 ;化合物C中显正价的是碘元素;
;化合物C中显正价的是碘元素;