��Ŀ����
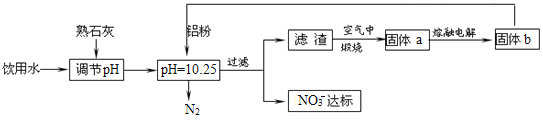
����Ŀ������ˮ��������ϵ����ϵ��ÿ���˵Ľ���������һ��Ũ�ȵ�NO3-�������ཡ������Σ����NO3-����������Ѫ�쵰���е�Fe��II����ʹ��ʧȥЯ������,Ϊ�˽�������ˮ��NO3-��Ũ�ȣ�ij��ȤС�������ͼ������
��ش��������⣺
��1������ѪҺ�����ȱ���������ӣ��ͻ����ȱ����ƶѪ���г����۵�ij����Ƭ�к�����������ϸС�Ļ�ԭ���ۣ���Щ����������θ�ᣨθ�����Ҫ�ɷ���HCl��������ת���������Ρ�д���÷�Ӧ�����ӷ���ʽ��____��
��2����֪���˺�õ���������һ�ֻ���������Һ�����ۺ�NO3-��Ӧ�����ӷ���ʽΪ__��
��3���÷�����ѡ����ʯ�ҵ���pH��������___��___��
��4����H2����ԭ��Ҳ�ɽ�������ˮ��NO3-��Ũ�ȣ���֪��Ӧ�еĻ�ԭ���������������ɲ������ѭ���������ԭ�������ӷ���ʽΪ___��
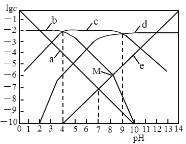
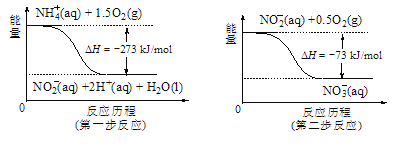
��5������ˮ�е�NO3-��Ҫ������NH4������֪���������õ������£�NH4������������Ӧ��������NO3-��������Ӧ�������仯ʾ��ͼ��ͼ����д��1molNH4��(aq)ȫ��������NO3-(aq)���Ȼ�ѧ����ʽ��____��
���𰸡�Fe+2H+=Fe2++H2�� 10Al+6NO3-+18H2O=10Al(OH)3+3N2��+6OH- �����Ca2+�������� ��Դ�ḻ���۸���� 5H2+2NO3-![]() N2+4H2O+2OH- NH4��(aq)��2O2(g)=2H��(aq)��NO3�� (aq)��H2O(l) ��H=-346kJ��mol��1
N2+4H2O+2OH- NH4��(aq)��2O2(g)=2H��(aq)��NO3�� (aq)��H2O(l) ��H=-346kJ��mol��1
��������
��������ˮ������ʯ�ҵ���pHֵ�������������ɵ������������������˵õ��������������������ڿ���������������������ˮ��������ڵ��������õ���������ѭ�����á�
(1) ����θ��ijɷּ���������ķ�Ӧԭ���������ɣ��������ᷴӦ�������Ȼ�������������
��2����������������ӷ���������ԭ��Ӧ���ɹ��壬�����Ϊ���������������ᱻ��ԭΪ������
��3��ѡ����ʯ�ҵ���pH��ԭ����Դ�ḻ���۸���ˣ����������Ӷ���������ע��pH������С������ֱ�ӷ���Al������ķ�Ӧ��
��4����H2����ԭ��Ҳ�ɽ�������ˮ��NO3-��Ũ�ȣ���Ӧ�еĻ�ԭ���������������ɲ������ѭ���������Ϊˮ�͵�����
��5����ͼ��֪����һ���Ȼ�ѧ��ӦΪNH4+��aq��+1.5O2��g��=2H+��aq��+NO2-��aq��+H2O��l����H=-273kJmol-1���ڶ����Ȼ�ѧ��ӦΪNO2-��aq��+0.5O2��g��=NO3-��aq����H=-73kJmol-1�����ø�˹���ɿɼ���1molNH4+��aq��ȫ��������NO3-��aq�����Ȼ�ѧ����ʽ��
��1��θ�����Ҫ�ɷ������ᣬ�����������ᷴӦ�����Ȼ�����������������ʽΪ��Fe+2HCl=FeCl2+H2����
�𰸣�Fe+2HCl�TFeCl2+H2����
��2����������������ӷ���������ԭ��Ӧ���ɹ��壬�����Ϊ���������������ᱻ��ԭΪ������������Һ�����ۺ�NO3-��Ӧ�����ӷ���ʽΪ10Al+6NO3-+18H2O=10Al(OH)3+3N2��+6OH-��
�𰸣�10Al+6NO3-+18H2O=10Al(OH)3+3N2��+6OH-��
��3��ѡ����ʯ�ҵ���pH��ԭ����Դ�ḻ���۸���ˣ����������Ӷ���������ע��pH������С������ֱ�ӷ���Al������ķ�Ӧ����������Al�Ĵ������ģ�
�𰸣������Ca2+������������Դ�ḻ���۸���ˣ�
��3��H2����ԭ����ˮ��NO3-����Ӧ�еĻ�ԭ���������������ɲ������ѭ���������Ϊˮ�͵������÷�ӦΪ5H2+2NO3-![]() N2+4H2O+2OH-��
N2+4H2O+2OH-��
�𰸣�5H2+2NO3-![]() N2+4H2O+2OH-��
N2+4H2O+2OH-��
��4����ͼ��֪����һ���Ȼ�ѧ��ӦΪNH4+��aq��+1.5O2��g��=2H+��aq��+NO2-��aq��+H2O��l����H=-273kJmol-1�٣��ڶ����Ȼ�ѧ��ӦΪNO2-��aq��+0.5O2��g��=NO3-��aq�� ��H=-73kJmol-1�ڣ��ɸ�˹���ɿ�֪��+�ڵ�NH4��(aq)��2O2(g)=2H��(aq)��NO3�� (aq)��H2O(l) ��H=-346kJ��mol��1��
�𰸣�NH4��(aq)��2O2(g)=2H��(aq)��NO3�� (aq)��H2O(l) ��H=-346kJ��mol��1��