题目内容
2.下列叙述中正确的是( )| A. | 常温常压下含有NA个原子的氦气体积约为22.4L | |
| B. | 常温常压下,O2和O3的混合物16g中约含有6.02×1023个氧原子 | |
| C. | 在0℃,101KPa时,22.4L氢气中含有NA个氢原子 | |
| D. | 标准状况下,33.6LH2O含有1.5NA个H2O分子 |
分析 A.含有NA个原子的氦气为1mol,常温常压下,气体摩尔体积大于22.4L/mol;
B.O2和O3的混合物16g,则氧原子质量为16g,根据n=$\frac{m}{M}$计算氧原子物质的量,再根据N=nNA计算氧原子数目;
C.在0℃,101KPa时,22.4L氢气为1mol,含有2mol氢原子;
D.标况下,水不是气体,33.6LH2O的物质的量远远大于1.5mol.
解答 解:A.含有NA个原子的氦气为1mol,常温常压下,气体摩尔体积大于22.4L/mol,则氦气体积大于22.4L,故A错误;
B.O2和O3的混合物16g,则氧原子质量为16g,氧原子物质的量为$\frac{16g}{16g/mol}$=1mol,则约含有6.02×1023个氧原子,故B正确;
C.在0℃,101KPa时,22.4L氢气为1mol,含有2mol氢原子,含有2NA个氢原子,故C错误;
D.标况下,水不是气体,33.6LH2O的物质的量远远大于1.5mol,故D错误,
故选:B.
点评 本题考查物质的量有关计算,难度不大,注意气体摩尔体积的属于体积与对象.

练习册系列答案
 巧学巧练系列答案
巧学巧练系列答案
相关题目
13.下列式子书写正确的是( )
| A. | 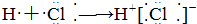 | B. | 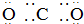 | ||
| C. | 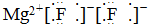 | D. |  |
10.在一定条件下,使CO和O2的混合气体30g充分反应,所得混合物在常温下跟足量的Na2O2固体反应,结果固体增重14g,下列关于混合气体的描述不正确的是( )
| A. | 原混合气体的平均摩尔质量为30g/mol | |
| B. | 原混合气体中CO和O2的物质的量之比为1:1 | |
| C. | 反应后的混合气体含有O2和CO2 | |
| D. | 反应后O2的物质的量比反应前的多 |
10.下列说法正确的是( )
| A. | 碱土金属元素是 IA 族元素 | B. | 被称为“生命元素”的是15号元素P | ||
| C. | 稀有气体元素都是非金属元素 | D. | 氕、氘、氚均可用做制造氢弹的原料 |