题目内容
2.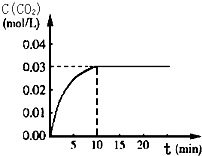 向某一容积为5L的密闭容器中,加入 0.2mol CO和0.2mol H2O,在800℃和催化剂存在的条件下,发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g)△H>0,反应中CO2的浓度随时间变化关系如图所示:
向某一容积为5L的密闭容器中,加入 0.2mol CO和0.2mol H2O,在800℃和催化剂存在的条件下,发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g)△H>0,反应中CO2的浓度随时间变化关系如图所示:(1)由图中数据可知,反应从开始至达到平衡时,CO的化学反应速率v(CO)=0.003mol/(L.min); H2的物质的量浓度c(H2)=0.03mol/L;该温度下此反应的平衡常数K=9.
(2)判断该反应是否达到平衡状态的依据是①③(填序号).
①CO减少的化学反应速率和CO2减少的化学反应速率相等
②CO、H2O、CO2、H2的浓度都相等
③CO、H2O、CO2、H2的浓度都不再发生变化
④正、逆反应速率都为0
(3)若开始时向该容器中加入CO、H2O(g)、CO2和H2各0.1mol,在相同条件下,反应达到平衡时,水蒸气的物质的量浓度c(H2O)=0.01mol/L.
分析 (1)根据v=$\frac{△c}{△t}$计算二氧化碳的平均反应速率,再结合同一时间段内同一可逆反应中,各物质的反应速率之比等于其计量数之比计算一氧化碳的平均反应速率;反应达到平衡状态时,二氧化碳的物质的量浓度等于氢气的物质的量浓度;根据平衡常数指各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值进行解答;
(2)化学反应达到平衡状态时,正逆反应速率相等,各物质的浓度不变,由此衍生的一些物理量也不变;
(3)如果一开始加入0.1mol的CO、0.1mol的H2O、0.1mol的CO2和0.1mol的H2,与开始时加入0.2mol CO和0.2mol H2O为等效平衡,则两种条件下,达到平衡状态时其水的物质的量浓度相等.
解答 解:(1)加入0.2mol的CO和0.2mol的H2O,则起始浓度c(CO)=c(H2O)=$\frac{0.2mol}{5L}$=0.04mol/L,平衡时c(CO2)=0.03mol/L,则
CO(g)+H2O(g)?CO2(g)+H2(g)
起始浓度/mol•L-1 :0.04 0.04 0 0
转化浓度/mol•L-1 :0.03 0.03 0.03 0.03
平衡浓度/mol•L-1 :0.01 0.01 0.03 0.03
v(CO2)=$\frac{△c}{△t}$=$\frac{0.03mol/L}{10min}$=0.003mol/(L.min),反应达到平衡状态时,c(CO2)=c(H2)=0.03mol/L,K=$\frac{c(CO{\;}_{2})•c(H{\;}_{2})}{c(CO)•c(H{\;}_{2}O)}$=$\frac{0.03×0.03}{0.01×0.01}$=9;
故答案为:0.003mol/(L.min);0.03mol/L;9;
(2)化学反应达到平衡状态时,正逆反应速率相等,各物质的浓度不变,由此衍生的一些物理量也不变,
①CO减少的速率和CO2减少的速率相等,该反应的正逆反应速率相等,所以该反应达到平衡状态,故正确;
②根据图象知,该反应达到平衡状态时,c(CO2)=c(H2)=0.03mol/L,则c(CO)=c(H2O)=0.01mol/L,当CO、H2O、CO2、H2等浓度都相等时,该反应未达到平衡状态,故错误;
③CO、H2O、CO2、H2的浓度都不再发生变化时,该反应达到平衡状态,故正确;
④该条件下,可逆反应达到平衡状态时,正逆反应速率相等但不等于0,故错误;
故选①③;
(3)如果一开始加入0.1mol的CO、0.1mol的H2O、0.1mol的CO2和0.1mol的H2,与开始时加入0.2mol CO和0.2mol H2O为等效平衡,则两种条件下,达到平衡状态时其水的物质的量浓度相等,所以达到平衡状态时,c(H2O)=$\frac{0.2mol-0.003mol/(L.min)×10min×5L}{5L}$═0.01mol/L,
故答案为:0.01mol/L.
点评 本题考查了化学平衡状态的判断、平衡浓度的计算等知识点,明确可逆反应平衡状态的判断依据、反应速率的计算公式即可解答,正确理解等效平衡,为学习难点.

| A. | NaCl+H2O═HCl+NaOH | B. | Cu+H2SO4═CuSO4+H2↑ | ||
| C. | 4HNO3═2H2O+4NO2↑+O2 | D. | 3Fe+4H20(g)═Fe3O4+4H2 |
| A. | 原子半径:As>Cl>P | B. | 热稳定性HCl>HBr>AsH3 | ||
| C. | 酸性:H3AsO4>H2SO4>H3PO4 | D. | 还原性:S2->Cl->Br- |
| A. | 一定是化合物 | B. | 可能是单质,可能是化合物 | ||
| C. | 一定是单质 | D. | 一定是不同的单质 |
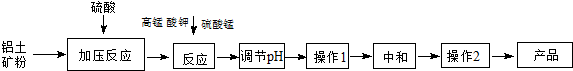
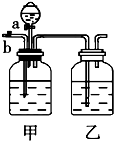 实验室用下列反应制取CO2和CO:H2C2O4$\stackrel{浓硫酸}{→}$CO2+CO+H2O,然后用如图所示装置将CO2和CO进行分离和干燥,已知分液漏斗中为稀硫酸,甲瓶中为NaOH溶液.试回答下列各题:
实验室用下列反应制取CO2和CO:H2C2O4$\stackrel{浓硫酸}{→}$CO2+CO+H2O,然后用如图所示装置将CO2和CO进行分离和干燥,已知分液漏斗中为稀硫酸,甲瓶中为NaOH溶液.试回答下列各题: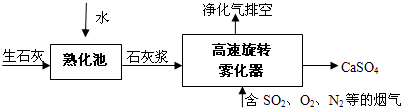 500℃时,在催化剂存在条件下,分别将2mol SO2和1mol O2置于恒压容器I和恒容容器II中(两容器起始容积相同),充分反应,二者均达到平衡后:
500℃时,在催化剂存在条件下,分别将2mol SO2和1mol O2置于恒压容器I和恒容容器II中(两容器起始容积相同),充分反应,二者均达到平衡后: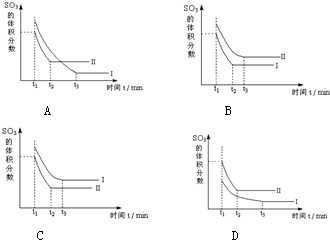
 工业上常用铁质容器盛装冷浓硫酸.为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:
工业上常用铁质容器盛装冷浓硫酸.为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动: