题目内容
17.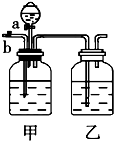 实验室用下列反应制取CO2和CO:H2C2O4$\stackrel{浓硫酸}{→}$CO2+CO+H2O,然后用如图所示装置将CO2和CO进行分离和干燥,已知分液漏斗中为稀硫酸,甲瓶中为NaOH溶液.试回答下列各题:
实验室用下列反应制取CO2和CO:H2C2O4$\stackrel{浓硫酸}{→}$CO2+CO+H2O,然后用如图所示装置将CO2和CO进行分离和干燥,已知分液漏斗中为稀硫酸,甲瓶中为NaOH溶液.试回答下列各题:(1)乙瓶中装的是浓H2SO4;
(2)关闭分液漏斗活塞a,打开b,通入混合气体,在右端收集到的气体是CO,甲中反应的离子方程式为2OH-+CO2=CO32-+H2O;
(3)通入气体结束后,得到另一种气体的方法是:关闭活塞b(填写a或b,下空同)打开a,在右端收集气体,此时甲中反应的离子方程式为CO32-+2H+=CO2↑+H2O.
分析 H2C2O4$\stackrel{浓硫酸}{→}$CO2+CO+H2O,草酸分解生成二氧化碳、一氧化碳等,用氢氧化钠吸收二氧化碳,可用浓硫酸干燥气体.
(1)应先通过氢氧化钠,先干燥的话会引入水蒸气;
(2)用氢氧化钠吸收二氧化碳,右端收集得到CO;
(3)碳酸钠与硫酸反应生成二氧化碳.
解答 解:(1)应先通过氢氧化钠,先干燥的话会引入水蒸气,乙瓶装浓H2SO4,故答案为:浓H2SO4;
(2)用氢氧化钠吸收二氧化碳,离子方程式为:2OH-+CO2=CO32-+H2O,右端收集得到CO,故答案为:CO;2OH-+CO2=CO32-+H2O;
(3)关闭活塞b,打开a,碳酸钠与硫酸反应生成二氧化碳,离子方程式为CO32-+2H+=CO2↑+H2O,故答案为:b、a;CO32-+2H+=CO2↑+H2O.
点评 本题考查气体的净化和干燥,侧重于学生的分析能力和实验能力的考查,为高频考点,注意把握实验的方法、步骤和使用的仪器,注重相关基础知识的积累,难度不大.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案
相关题目
11.下列图示能达到实验目的是( )
| A. |  乙酸乙酯的制备 | B. | 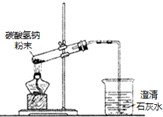 检验碳酸氢钠受热分解的CO2 | ||
| C. | 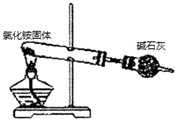 制备氨气 | D. | 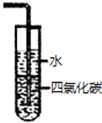 吸收氯气并防倒吸 |
12.下列有关说法中错误的是( )
| A. | 氢氟酸不能盛放在玻璃试剂瓶中 | |
| B. | 玻璃、水晶、陶瓷的主要成分均是硅酸盐 | |
| C. | 灼烧NaOH固体时不能使用瓷坩埚,因为坩埚中的SiO2能与NaOH反应 | |
| D. | 由沙子制备光伏材料时的反应之一为SiO2+2C $\frac{\underline{\;高温\;}}{\;}$Si+2CO↑ |
5. 某化学兴趣小组的同学为制取少量溴乙烷,查阅资料得知:
某化学兴趣小组的同学为制取少量溴乙烷,查阅资料得知:
NaBr+H2SO4→HBr+NaHSO4
CH3CH2OH+HBr$\stackrel{△}{→}$CH3CH2Br+H2O
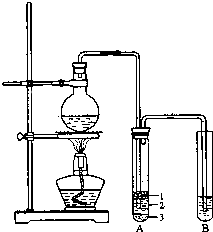
化学兴趣小组根据实验原理设计如图的装置.根据题意完成下列填空:有关数据列表如下:
(1)圆底烧瓶中加入的反应物是溴化钠、乙醇和2:1的硫酸.配制体积比2:1的硫酸所用的仪器为abc选填编号)
a.烧杯 b.玻璃棒 c.量筒 d.容量瓶 e.滴定管
(2)将生成物导入盛有冰水混合物的试管A中,试管A中的物质分为三层(如图所示),产物在第3层;
(3)用浓的硫酸进行实验,若试管A中获得的有机物呈棕黄色,除去其中杂质应加入d选填编号)然后再进行分液一步操作即可;
a.无水氯化钙 b.硝酸银溶液 c.四氯化碳 d.亚硫酸钠溶液
(4)实验过程中,同学发现仪器连接部分有漏气现象,老师建议把上述装置中的仪器连接部分都改成标准玻璃接口,其原因是:反应会产生Br2,腐蚀橡胶;
(5)假设最初取用的无水乙醇是57.5mL,最后得到的纯净的溴乙烷是52.0mL,则溴乙烷的产率为66.8%.
 某化学兴趣小组的同学为制取少量溴乙烷,查阅资料得知:
某化学兴趣小组的同学为制取少量溴乙烷,查阅资料得知:NaBr+H2SO4→HBr+NaHSO4
CH3CH2OH+HBr$\stackrel{△}{→}$CH3CH2Br+H2O
化学兴趣小组根据实验原理设计如图的装置.根据题意完成下列填空:有关数据列表如下:
| 乙醇 | 溴乙烷 | |
| 状态 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.8 | 1.4 |
| 沸点/℃ | 78.5 | 119.0 |
| 熔点/℃ | -130 | 38.4 |
a.烧杯 b.玻璃棒 c.量筒 d.容量瓶 e.滴定管
(2)将生成物导入盛有冰水混合物的试管A中,试管A中的物质分为三层(如图所示),产物在第3层;
(3)用浓的硫酸进行实验,若试管A中获得的有机物呈棕黄色,除去其中杂质应加入d选填编号)然后再进行分液一步操作即可;
a.无水氯化钙 b.硝酸银溶液 c.四氯化碳 d.亚硫酸钠溶液
(4)实验过程中,同学发现仪器连接部分有漏气现象,老师建议把上述装置中的仪器连接部分都改成标准玻璃接口,其原因是:反应会产生Br2,腐蚀橡胶;
(5)假设最初取用的无水乙醇是57.5mL,最后得到的纯净的溴乙烷是52.0mL,则溴乙烷的产率为66.8%.

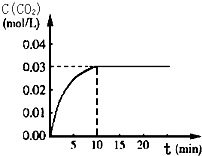 向某一容积为5L的密闭容器中,加入 0.2mol CO和0.2mol H2O,在800℃和催化剂存在的条件下,发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g)△H>0,反应中CO2的浓度随时间变化关系如图所示:
向某一容积为5L的密闭容器中,加入 0.2mol CO和0.2mol H2O,在800℃和催化剂存在的条件下,发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g)△H>0,反应中CO2的浓度随时间变化关系如图所示:
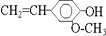 ,它不可能具有的性质是( )
,它不可能具有的性质是( )