��Ŀ����
10����ҵ�����������������������ȡ������ú�����Fe2+��Fe3+������������Һ�����ȵ�һ���¶ȣ����裬����һ�������������Һ����������Һ������Һ�����ɻ��Զ������̣�������Һ��pH����Ӧһ��ʱ�䣬Fe ��OH�� 3�Ͷ������̷��������������ã����յõ�������������Ʒ��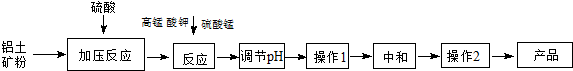
��1��KMnO4���Ƚ�Fe2+����ΪFe3+���䱾������ԭΪMnO2����Ӧ�����ӷ���ʽΪMnO4-+3Fe2++4H+=3Fe3++MnO2+2H2O��
��2��д�����������Һ����������Һ��Ӧ�Ļ�ѧ����ʽ2KMnO4+3MnSO4+2H2O=5MnO2��+K2SO4+2H2SO4��ʵ��֤����n��MnO2��/n��Fe��������4��1ʱ������Ч���Ϻã�����Һ���������Ӻ�������Ũ�Ⱦ�Ϊ0.03mol/L��Ϊ�ﵽ�Ϻõij���Ч����ÿ1L��ҺӦ���������ص����ʵ���Ϊ0.102mol��
��3������pH��������ʹ������ת��Ϊ��������������ȥ��
��4������1������Ϊ���ˣ�����2������Ϊ����Ũ������ȴ�ᾧ������ϴ�ӣ�
��5�������йع��յ�˵����ȷ����ABC��������ĸ��ţ�
A����������Һ���ټ���������۵ȵ���pH
B����Һ�ļ���Խǿ�������Ч��Խ�ã���ͬʱ��Ӱ���������IJ���
C�����Զ�������������Ӧ���ˣ�����ʱ����ȥ���ʽϵͣ�����ʱ�����ӳɱ�
D������ֱ������Һ�м���������̷�ĩ�Գ�ȥFe ��OH�� 3��
���� ��ҵ�����������������������ȡ������ú�����Fe2+��Fe3+������������Һ�����ȵ�һ���¶ȣ����裬����һ�������������Һ����������Һ������Һ�����ɻ��Զ������̣�������Һ��pH����Ӧһ��ʱ�䣬Fe��OH��3�Ͷ������̷��������������ã����յõ�������������Ʒ��
��1��KMnO4���Ƚ�Fe2+����ΪFe3+���䱾������ԭΪMnO2������ԭ���غ�͵���غ���д���ӷ���ʽ��
��2������������ԭ��Ӧ�л��ϼ�������ȣ���д����ѧ����ʽΪ2KMnO4+3MnSO4+2H2O=5MnO2��+K2SO4+2H2SO4��������ӷ���ʽ�ͻ�ѧ����ʽ������ϵ���㣻
��3������������ˮ�ⷴӦ��������������
��4������1Ϊ���ˣ�����2Ϊ�����ᾧ��
��5��A�����������ᷴӦ��������pH�����ã����Ҳ������µ����ʣ�
B��������������������Ӧ������������������
C�����Զ������̲���ʱ����ȥ���ʽϵͣ�
D��ֱ������Һ�м���������̷�ĩ��������̫�ͣ�
��� �⣺��ҵ�����������������������ȡ������ú�����Fe2+��Fe3+������������Һ�����ȵ�һ���¶ȣ����裬����һ�������������Һ����������Һ������Һ�����ɻ��Զ������̣�������Һ��pH����Ӧһ��ʱ�䣬Fe��OH��3�Ͷ������̷��������������ã����յõ�������������Ʒ��
��1��KMnO4���Ƚ�Fe2+����ΪFe3+���䱾������ԭΪMnO2������ԭ���غ�͵���غ���д���ӷ���ʽΪ��MnO4-+3Fe2++4H+=3Fe3++MnO2+2H2O��
�ʴ�Ϊ��MnO4-+3Fe2++4H+=3Fe3++MnO2+2H2O��
��2���������֪���������Һ����������Һ��Ӧ���ɻ��Զ������̣�����������ԭ��Ӧ�л��ϼ�������ȣ���д����ѧ����ʽΪ2KMnO4+3MnSO4+2H2O=5MnO2��+K2SO4+2H2SO4������Һ���������Ӻ�������Ũ�Ⱦ�Ϊ0.03mol/L����Һ�к���Fe2+���ʵ���Ϊ0.03mol��������ҺPHʹ������ȫ��������n��Fe��=0.06mol
MnO4-+3Fe2++4H+=3Fe3++MnO2+2H2O��
0.01mol 0.03mol 0.01mol
n��MnO2��/n��Fe��������4��1ʱ������Ч���Ϻã���n��MnO2��=0.06mol��4=0.24mol��
��Ӧ�����ɶ����������ʵ���=0.24mol-0.01mol=0.23mol�����ĸ���������ʵ�����
2KMnO4+3MnSO4+2H2O=5MnO2��+K2SO4+2H2SO4��
2 5
n 0.23mol
n=0.0.092mol
Ϊ�ﵽ�Ϻõij���Ч����ÿ1L��ҺӦ���������ص����ʵ���=0.092mol+0.01mol=0102mol��
�ʴ�Ϊ��2KMnO4+3MnSO4+2H2O=5MnO2��+K2SO4+2H2SO4��0.102mol��
��3������������ˮ�ⷴӦ����������������������ҺPH��ʹ��ҺPH����ʱ����ʹ������ת��Ϊ��������������ȥ��
�ʴ�Ϊ��ʹ������ת��Ϊ��������������ȥ��
��4������������Ϣ����Ӧһ��ʱ�䣬�������̺�Fe ��OH�� 3���������������ã���֪����1Ϊ���ˣ�����2Ϊ���˺���Һ����Ũ������ȴ�ᾧ������ϴ�ӣ�
�ʴ�Ϊ�����ˣ�����Ũ������ȴ�ᾧ������ϴ�ӣ�
��5��A�����������ᷴӦ������Һ���ټ���������ۿ�����pH�����ã����Ҳ������µ����ʣ���A��ȷ��
B�������Һ�ļ���̫ǿ��������������Ӧ���������������������²��ʽϵͣ���B��ȷ��
C�����Զ������̲���ʱ������ȫ��ȥ��������������ȥ���ʽϵͣ�����ʱ�����ӳɱ�����C��ȷ��
D��ֱ������Һ�м���������̷�ĩ��������̫�ͣ���D����
�ʴ�Ϊ��ABC��
���� ���⿼���Ϊ�ۺϣ�������ʵ��Ʊ����̡����ӷ���ʽ����д��������ԭ��Ӧ�����ʵķ�����ᴿ�����⣬����Ŀ�Ѷ��еȣ�����ע������Ʊ�ԭ����ʵ�����̣�

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�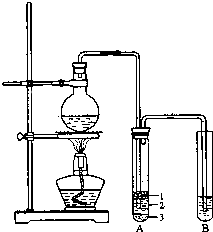 ij��ѧ��ȤС���ͬѧΪ��ȡ���������飬�������ϵ�֪��
ij��ѧ��ȤС���ͬѧΪ��ȡ���������飬�������ϵ�֪��NaBr+H2SO4��HBr+NaHSO4
CH3CH2OH+HBr$\stackrel{��}{��}$CH3CH2Br+H2O
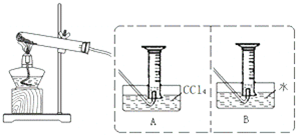
��ѧ��ȤС�����ʵ��ԭ�������ͼ��װ�ã������������������գ��й������б����£�
| �Ҵ� | ������ | |
| ״̬ | ��ɫҺ�� | ��ɫҺ�� |
| �ܶ�/g•cm-3 | 0.8 | 1.4 |
| �е�/�� | 78.5 | 119.0 |
| �۵�/�� | -130 | 38.4 |
a���ձ� b�������� c����Ͳ d������ƿ e���ζ���
��2���������ﵼ��ʢ�б�ˮ�������Թ�A�У��Թ�A�е����ʷ�Ϊ���㣨��ͼ��ʾ���������ڵ�3�㣻
��3����Ũ���������ʵ�飬���Թ�A�л�õ��л�����ػ�ɫ����ȥ��������Ӧ����dѡ���ţ�Ȼ���ٽ��з�Һһ���������ɣ�
a����ˮ�Ȼ��� b����������Һ c�����Ȼ�̼ d������������Һ
��4��ʵ������У�ͬѧ�����������Ӳ�����©��������ʦ���������װ���е��������Ӳ��ֶ��ijɱ������ӿڣ���ԭ���ǣ���Ӧ�����Br2����ʴ��
��5���������ȡ�õ���ˮ�Ҵ���57.5mL�����õ��Ĵ�������������52.0mL����������IJ���Ϊ66.8%��
| A�� | ú�ĸ����ʯ�͵ķ�������ڻ�ѧ�仯 | |
| B�� | 14C��������������ļ�����14C��12C��Ϊͬ�������� | |
| C�� | ����������������������ͳɷ���ʯ������ȡ�IJ��ͳɷ���ͬ | |
| D�� | ������ע��Һ���ܲ��������ЧӦ�������ڽ��� |
 Ϊ̽��Fe��NO3��2���������ȷֽ����Ͳ�������ʣ�ij��ѧС�鿪չ����̽����ѧϰ��
Ϊ̽��Fe��NO3��2���������ȷֽ����Ͳ�������ʣ�ij��ѧС�鿪չ����̽����ѧϰ��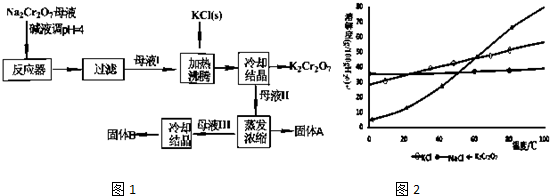
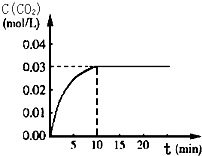 ��ijһ�ݻ�Ϊ5L���ܱ������У����� 0.2mol CO��0.2mol H2O����800��ʹ������ڵ������£��������·�Ӧ��CO��g��+H2O��g��?CO2��g��+H2��g����H��0����Ӧ��CO2��Ũ����ʱ��仯��ϵ��ͼ��ʾ��
��ijһ�ݻ�Ϊ5L���ܱ������У����� 0.2mol CO��0.2mol H2O����800��ʹ������ڵ������£��������·�Ӧ��CO��g��+H2O��g��?CO2��g��+H2��g����H��0����Ӧ��CO2��Ũ����ʱ��仯��ϵ��ͼ��ʾ��