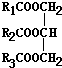题目内容
羧酸:
(1)定义: .
(2)物理性质:随碳链增长,沸点 溶解度 酸性 .
(3)化学性质:与乙酸相似
(4)几种重要的羧酸:
①甲酸:HCOOH,既含有羧基又含有醛基.
②高级脂肪酸:不饱和:油酸: 态
饱和:硬脂酸: 态; 软脂酸: 态.
(1)定义:
(2)物理性质:随碳链增长,沸点
(3)化学性质:与乙酸相似
(4)几种重要的羧酸:
①甲酸:HCOOH,既含有羧基又含有醛基.
②高级脂肪酸:不饱和:油酸:
饱和:硬脂酸:
考点:羧酸简介
专题:有机物分子组成通式的应用规律
分析:(1)羧酸中含有羧基;
(2)羧酸属于分子晶体,碳原子数越多,分子量越大,分子间作用力越强,沸点越高;羧酸的溶解度与氢键的形成的几率有关;酸性的强弱取决于羟基氢断裂的难易程度;
(4)②不饱和高级脂肪酸烃基中含有不饱和键,为液态;
饱和高级脂肪酸烃基中不含不饱和键,为固态.
(2)羧酸属于分子晶体,碳原子数越多,分子量越大,分子间作用力越强,沸点越高;羧酸的溶解度与氢键的形成的几率有关;酸性的强弱取决于羟基氢断裂的难易程度;
(4)②不饱和高级脂肪酸烃基中含有不饱和键,为液态;
饱和高级脂肪酸烃基中不含不饱和键,为固态.
解答:
解:(1)羧酸中含有羧基,烃基与羧基相连得到的产物就是羧酸,
故答案为:烃基和羧基相连构成的有机化合物;
(2)羧酸属于分子晶体,随碳链增长,分子量越大,分子间作用力越强,沸点越高;羧酸的溶解度与氢键的形成的几率有关,随碳链增长,羧酸分子与水分子之间形成氢键的几率减小,所以溶解性依次减小;羧酸的酸性的强弱取决于羟基氢断裂的难易程度,烃基越大对羧基中O-H键的推电子作用越强,O-H键越难断裂,所以酸性,随碳链增长,逐渐减弱;
故答案为:升高;降低;减弱;
(4)②不饱和高级脂肪酸烃基中含有不饱和键,为液体,油酸属于不饱和高级脂肪酸,所以属于液态;
饱和高级脂肪酸烃基中不含不饱和键,为固态,硬脂酸、软脂酸都是饱和高级脂肪酸,所以属于固态;
故答案为:液;固;固.
故答案为:烃基和羧基相连构成的有机化合物;
(2)羧酸属于分子晶体,随碳链增长,分子量越大,分子间作用力越强,沸点越高;羧酸的溶解度与氢键的形成的几率有关,随碳链增长,羧酸分子与水分子之间形成氢键的几率减小,所以溶解性依次减小;羧酸的酸性的强弱取决于羟基氢断裂的难易程度,烃基越大对羧基中O-H键的推电子作用越强,O-H键越难断裂,所以酸性,随碳链增长,逐渐减弱;
故答案为:升高;降低;减弱;
(4)②不饱和高级脂肪酸烃基中含有不饱和键,为液体,油酸属于不饱和高级脂肪酸,所以属于液态;
饱和高级脂肪酸烃基中不含不饱和键,为固态,硬脂酸、软脂酸都是饱和高级脂肪酸,所以属于固态;
故答案为:液;固;固.
点评:本题考查了羧酸的定义、性质、结构,侧重考查学生对羧酸基础知识的掌握,依据课本即可解答,难度不大.

练习册系列答案
相关题目
下列反应属于吸热反应的是( )
| A、葡萄糖在人体内氧化供能 |
| B、氢气在氧气中燃烧 |
| C、氢氧化钡晶体与氯化铵晶体反应 |
| D、氢氧化钾溶液和硫酸中和 |
下列试剂中,不能贮存在玻璃瓶中的是( )
| A、浓硫酸 | B、氢氟酸 |
| C、浓氢氧化钠溶液 | D、硝酸银溶液 |
下列物质中,不含醛基的是( )
| A、C6H5CHO |
| B、CHOOC2H5 |
| C、(CH3)3CCH2OH |
| D、(CH3)2CH-CH=O |
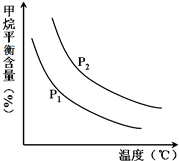 氮的固定是指将氮元素由游离态转化为化合态的过程.据报道,常温、常压、光照条件下,N2在掺有少量氧化铁的二氧化钛催化剂表面能与水发生反应,生成的主要产物为NH3,相应的热化学方程式为:2N2(g)+6H2O(l)?4NH3(g)+3O2(g)△H=+1530.0kJ/mol.目前工业合成氨的原理是:N2(g)+3H2(g)?2NH3(g)△H=-93.0kJ/mol.
氮的固定是指将氮元素由游离态转化为化合态的过程.据报道,常温、常压、光照条件下,N2在掺有少量氧化铁的二氧化钛催化剂表面能与水发生反应,生成的主要产物为NH3,相应的热化学方程式为:2N2(g)+6H2O(l)?4NH3(g)+3O2(g)△H=+1530.0kJ/mol.目前工业合成氨的原理是:N2(g)+3H2(g)?2NH3(g)△H=-93.0kJ/mol.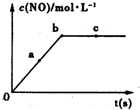 氮元素的单质及其化合物的研究和应用在工农业生产中有着非常重要的地位.工业制硝酸的主要反应之一是4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-akJ?mol-1(a>0)
氮元素的单质及其化合物的研究和应用在工农业生产中有着非常重要的地位.工业制硝酸的主要反应之一是4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-akJ?mol-1(a>0)