题目内容
写出下列反应的离子方程式:
(1)石灰石溶于稀硝酸
(2)电解氯化钠的水溶液
(3)氧化铜溶于氢溴酸
(4)氯气通入水中
(5)氯气通入氢氧化钠溶液中 .
(1)石灰石溶于稀硝酸
(2)电解氯化钠的水溶液
(3)氧化铜溶于氢溴酸
(4)氯气通入水中
(5)氯气通入氢氧化钠溶液中
考点:离子方程式的书写
专题:离子反应专题
分析:(1)石灰石和硝酸反应生成硝酸钙、二氧化碳和水;
(2)电解氯化钠溶液时生成氯气、氢气和氢氧化钠;
(3)氧化铜和氢溴酸反应生成溴化铜和水;
(4)氯气和水反应生成盐酸和次氯酸;
(5)氯气和氢氧化钠反应生成氯化钠、次氯酸钠和水.
(2)电解氯化钠溶液时生成氯气、氢气和氢氧化钠;
(3)氧化铜和氢溴酸反应生成溴化铜和水;
(4)氯气和水反应生成盐酸和次氯酸;
(5)氯气和氢氧化钠反应生成氯化钠、次氯酸钠和水.
解答:
解:(1)石灰石和硝酸反应生成硝酸钙、二氧化碳和水,离子方程式为CaCO3+2H+=Ca2++H2O+CO2↑,故答案为:CaCO3+2H+=Ca2++H2O+CO2↑;
(2)电解氯化钠溶液时生成氯气、氢气和氢氧化钠,离子方程式为2Cl-+2H2O
2OH-+Cl2↑+H2↑,故答案为:2Cl-+2H2O
2OH-+Cl2↑+H2↑;
(3)氧化铜和氢溴酸反应生成溴化铜和水,离子方程式为CuO+2H+=Cu2++H2O,故答案为:CuO+2H+=Cu2++H2O;
(4)氯气和水反应生成盐酸和次氯酸,离子方程式为Cl2+H2O=Cl-+HClO+H+,故答案为:Cl2+H2O=Cl-+HClO+H+;
(5)氯气和氢氧化钠反应生成氯化钠、次氯酸钠和水,离子方程式为Cl2+2OH-=Cl-+ClO-+H2O,故答案为:Cl2+2OH-=Cl-+ClO-+H2O.
(2)电解氯化钠溶液时生成氯气、氢气和氢氧化钠,离子方程式为2Cl-+2H2O
| ||
| ||
(3)氧化铜和氢溴酸反应生成溴化铜和水,离子方程式为CuO+2H+=Cu2++H2O,故答案为:CuO+2H+=Cu2++H2O;
(4)氯气和水反应生成盐酸和次氯酸,离子方程式为Cl2+H2O=Cl-+HClO+H+,故答案为:Cl2+H2O=Cl-+HClO+H+;
(5)氯气和氢氧化钠反应生成氯化钠、次氯酸钠和水,离子方程式为Cl2+2OH-=Cl-+ClO-+H2O,故答案为:Cl2+2OH-=Cl-+ClO-+H2O.
点评:本题考查了离子方程式的书写,明确物质之间的反应及离子方程式的书写规则是解本题关键,注意次氯酸是弱电解质,要写化学式,为易错点.

练习册系列答案
相关题目
下列物质结构的化学用语或模型正确的是( )
| A、乙醇的结构简式:CH3CH2OH |
B、HF的电子式: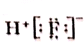 |
C、氯离子的结构示意图: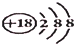 |
D、CH4分子的球棍模型: |
 一根细如发丝的光缆可以同时传导上千部电话,是铜导线传导能力的约100倍左右.“光缆无铜,盗割有罪”.试问:光缆主要是以
一根细如发丝的光缆可以同时传导上千部电话,是铜导线传导能力的约100倍左右.“光缆无铜,盗割有罪”.试问:光缆主要是以下列实验现象及相关的离子方程式均正确的是( )
| A、碳酸钙粉末中加人醋酸溶液,固体逐渐减少,生成无色气体 CaCO3+2H+=Ca2++CO2↑+H2O | ||
| B、向BaCl2溶液中通人SO2气体,出现白色沉淀 Ba2++SO2+H2O=BaSO4↓+2H+ | ||
C、向H2O2溶液中滴加酸化的KMnO4溶液,KMnO4溶液褪色 2MnO
| ||
| D、将等物质的量浓度、等体积的Ba(OH)2溶液和NaHSO4溶液混合,生成白色沉淀 Ba2++SO42-+H++OH-=BaSO4↓+H2O |
