��Ŀ����
 ��Ԫ�صĵ��ʼ��仯������о���Ӧ���ڹ�ũҵ���������ŷdz���Ҫ�ĵ�λ����ҵ���������Ҫ��Ӧ֮һ��4NH3��g��+5O2��g��?4NO��g��+6H2O��g����H=-akJ?mol-1��a��0��
��Ԫ�صĵ��ʼ��仯������о���Ӧ���ڹ�ũҵ���������ŷdz���Ҫ�ĵ�λ����ҵ���������Ҫ��Ӧ֮һ��4NH3��g��+5O2��g��?4NO��g��+6H2O��g����H=-akJ?mol-1��a��0����1�������4mol NH3��5mol O2���������У��ﵽƽ��ʱ�ų�����0.8akJ����ƽ��ʱNH3��ת����Ϊ
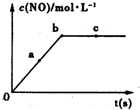
��2����һ�������£��ݻ��̶����ܱ������н���������Ӧ��NO��Ũ����ʱ���ϵ��ͼ��ʾ����NO��a��b��c����ķ�Ӧ����v��a������v��b�棩��v��c�����Ĵ�С��ϵ��
��3��t��ʱ�����ݻ��̶����ܱ������з���������Ӧ�������ڸ����ʵ�Ũ�������
| Ũ��/mol?L-1 \ʱ��/min | C��NH2�� | C��O2�� | C��NO�� | C��H2O�� |
| ����ʼ | 4.0 | 5.5 | 0 | 0 |
| ��2min | 3.2 | 4.5 | 0.8 | 1.2 |
| ��4min | 2.0 | 3.0 | 2.0 | 3.0 |
| ��6min | 2.0 | 3.0 | 2.0 | 3.0 |
�ڵ�2minʱ�ı����������ı������������
A�������¶� B�������������� C����Сѹǿ D��ʹ���˸�Ч����
�������4min��ͬ���¶��£�����ʼ�������м���NH3��O2��NO��H2O��g����Ũ�ȶ�Ϊ2mol/L����÷�Ӧ
��4�����᳧��β�����е��������������ֱ���ŷŽ���Ⱦ���������أ�H2NCONH2����һ�ַdz���Ҫ�ĸߵ����ʣ����¶�70-95��ʱ����ҵβ���е�NO��NO2������������Һ���գ�����ת��ΪN2��������NO��NO2���ߵ����ʵ�����Ӧ�Ļ�ѧ����ʽΪ
��5��Ŀǰ��ѧ��̽������ȼ�������еļ���Ƚ��������ﻹԭΪ������ˮ���䷴Ӧ����Ϊ��
CH4��g��+4NO2��g���T4NO��g��+CO2��g��+2H2O��g����H=-574kJ?mol-1
CH4��g��+4NO��g���T2N2��g��+CO2��g��+2H2O��g����H=-1160kj?mol-1
��1mol����ֱ�ӽ�NO2��ԭΪN2�Ļ��Ϊ
���㣺���ʵ�����Ũ����ʱ��ı仯����,�Ȼ�ѧ����ʽ,��ѧƽ���Ӱ������,��ѧƽ��ļ���
ר�⣺��ѧƽ��ר��
��������1�������Ȼ�ѧ����ʽ�����ʵ������ʱ���㷴Ӧ�İ������ʵ��������ת����=
���㣻
��2�����ݷ�Ӧ������һ�������淴Ӧ����Ũ�����ﵽƽ��״̬Ũ�Ȳ��������
��3�����ȸ���v=
����һ�������ķ�Ӧ���ʣ��ٸ���ͬһ���淴Ӧ�У�ͬһʱ����ڣ���Ԫ�صķ�Ӧ����֮�ȵ����������֮��ȷ�������ķ�Ӧ���ʣ�
���ȷ���ͼ�����ٸ������Ի�ѧƽ���Ӱ�������
�۸���Ũ�����뻯ѧƽ�ⳣ������Դ�С�ж��ƶ�����
��4������ԭ���غ���ƽ��д��ѧ����ʽ��
��5�����ݸ�˹���������㷴Ӧ���ʱ䣬������д�Ȼ�ѧ����ʽ��
| ������ |
| ��ʼ�� |
��2�����ݷ�Ӧ������һ�������淴Ӧ����Ũ�����ﵽƽ��״̬Ũ�Ȳ��������
��3�����ȸ���v=
| ��c |
| ��t |
���ȷ���ͼ�����ٸ������Ի�ѧƽ���Ӱ�������
�۸���Ũ�����뻯ѧƽ�ⳣ������Դ�С�ж��ƶ�����
��4������ԭ���غ���ƽ��д��ѧ����ʽ��
��5�����ݸ�˹���������㷴Ӧ���ʱ䣬������д�Ȼ�ѧ����ʽ��
���
�⣺��1�������4molNH3��5molO2���������У��ﵽƽ��ʱ�ų�����0.8akJ����
4NH3��g��+5O2��g��?4NO��g��+6H2O��g������H=-akJ?mol-1
��ʼ�� 4mol 5mol 0 0
�ʱ� 4mol aKJ
���� n 0.8aKJ
n=3.2mol
����ת����=
��100%=80%���ʴ�Ϊ��80%��
��2���ݻ��̶����ܱ������н���������Ӧ��NO��Ũ����ʱ���ϵ������֪�淴Ӧ���У�һ�������淴Ӧ����Ũ�����ﵽƽ��״̬Ũ�Ȳ��䣬��ʼͶ�ķ�Ӧ���Ӧ���Ũ������������ʹ�ϵΪ��v��a������v��b�棩=v��c������
�ʴ�Ϊ��v��a������v��b�棩=v��c������
��3���ٷ�Ӧ�ڵ�2min����4minʱ����v��O2��=
=0.75mol/��L��min�����ʴ�Ϊ��0.75mol/��L��min����
�ڸ����������2min����4minʱ���ʵ���Ũ�ȵı仯��֪����2min����4minʱ��Ӧ����������ƽ��������Ӧ�����ƶ������2minʱ�ı���������ʹ�ô�����Ӧ�����������ﵽƽ��״̬����ѡD��
�۵�4minʱ���������ʵ�Ũ�Ȳ��䣬˵���÷�Ӧ�ﵽƽ��״̬����ѧƽ�ⳣ��K=
=3.0�������4min��ͬ���¶��£�����ʼ�������м���NH3��O2��NO��H2O��g����Ũ�ȶ�Ϊ2moI/L��Q=
=2��3����ƽ��������Ӧ�����ƶ����ʴ�Ϊ������Ӧ������У�
��4�����¶�70-95��ʱ����ҵβ���е�NO��NO2������������Һ���գ�����ת��ΪN2��ͬʱ����CO2����������NO��NO2���ߵ����ʵ�����Ӧ�Ļ�ѧ����ʽΪ��
CO��NH2��2+NO+NO2
N2+CO2+2H2O��
�ʴ�Ϊ��CO��NH2��2+NO+NO2
N2+CO2+2H2O��
��5���������⣺��
CH4��g��+2NO2��g��=2NO��g��+
CO2��g��+H2O��g����H=
����-574kJ?mol-1��=-287kJ?mol-1��
CH4��g��+2NO��g��=N2��g��+
CO2��g��+H2O��g����H=
����-1160kJ?mol-1��=-580kJ?mol-1��
���ݸ�˹���ɷ�ӦCH4��g��+2NO2��g��=N2��g��+CO2��g��+2H2O��g�����Կ����Ǣ�+�ڣ�CH4��g��+2NO2��g��=N2��g��+CO2��g��+2H2O��g����H=-867kJ?mol-1��
���ԡ�H=-287kJ?mol-1-580kJ?mol-1=-867kJ?mol-1��
�ʴ�Ϊ��-867kJ?mol-1��
4NH3��g��+5O2��g��?4NO��g��+6H2O��g������H=-akJ?mol-1
��ʼ�� 4mol 5mol 0 0
�ʱ� 4mol aKJ
���� n 0.8aKJ
n=3.2mol
����ת����=
| 3.2mol |
| 4mol |
��2���ݻ��̶����ܱ������н���������Ӧ��NO��Ũ����ʱ���ϵ������֪�淴Ӧ���У�һ�������淴Ӧ����Ũ�����ﵽƽ��״̬Ũ�Ȳ��䣬��ʼͶ�ķ�Ӧ���Ӧ���Ũ������������ʹ�ϵΪ��v��a������v��b�棩=v��c������
�ʴ�Ϊ��v��a������v��b�棩=v��c������
��3���ٷ�Ӧ�ڵ�2min����4minʱ����v��O2��=
| 4.5mol/L-3mol/L |
| 4min-2min |
�ڸ����������2min����4minʱ���ʵ���Ũ�ȵı仯��֪����2min����4minʱ��Ӧ����������ƽ��������Ӧ�����ƶ������2minʱ�ı���������ʹ�ô�����Ӧ�����������ﵽƽ��״̬����ѡD��
�۵�4minʱ���������ʵ�Ũ�Ȳ��䣬˵���÷�Ӧ�ﵽƽ��״̬����ѧƽ�ⳣ��K=
| 24��36 |
| 24��35 |
| 24��26 |
| 24��25 |
��4�����¶�70-95��ʱ����ҵβ���е�NO��NO2������������Һ���գ�����ת��ΪN2��ͬʱ����CO2����������NO��NO2���ߵ����ʵ�����Ӧ�Ļ�ѧ����ʽΪ��
CO��NH2��2+NO+NO2
| ||
�ʴ�Ϊ��CO��NH2��2+NO+NO2
| ||
��5���������⣺��
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
CH4��g��+2NO��g��=N2��g��+
| 1 |
| 2 |
| 1 |
| 2 |
���ݸ�˹���ɷ�ӦCH4��g��+2NO2��g��=N2��g��+CO2��g��+2H2O��g�����Կ����Ǣ�+�ڣ�CH4��g��+2NO2��g��=N2��g��+CO2��g��+2H2O��g����H=-867kJ?mol-1��
���ԡ�H=-287kJ?mol-1-580kJ?mol-1=-867kJ?mol-1��
�ʴ�Ϊ��-867kJ?mol-1��
���������⿼���˷�Ӧ�����仯�ļ����˹����Ӧ�ã���ѧƽ���ƶ�ԭ���ķ����жϣ�ƽ�ⳣ������Ӧ���ʼ��㣬���ջ����ǹؼ�����Ŀ�ѶȽϴ�

��ϰ��ϵ�д�
 �������ϵ�д�
�������ϵ�д�
�����Ŀ
�ס������ֽ������ʱȽϣ�
�ټĵ����ۡ��е���ҵĵͣ�
�ڳ����£�������ˮ��Ӧ�ų��������Ҳ��ܣ�
������������Ӧ��ˮ������ԱȽϣ��ұȼ�ǿ��
�ܼס������缫��ϡ����Ϊ�������Һ���ԭ��أ��ҵ缫����������ݣ�
������Ŀ���ܹ�˵���ױ��ҵĽ�����ǿ���ǣ�������
�ټĵ����ۡ��е���ҵĵͣ�
�ڳ����£�������ˮ��Ӧ�ų��������Ҳ��ܣ�
������������Ӧ��ˮ������ԱȽϣ��ұȼ�ǿ��
�ܼס������缫��ϡ����Ϊ�������Һ���ԭ��أ��ҵ缫����������ݣ�
������Ŀ���ܹ�˵���ױ��ҵĽ�����ǿ���ǣ�������
| A���٢� | B���ڢ� | C���ڢ� | D���٢� |
����ʱ��������Һ��pH���������ʵ���Ũ�ȹ�ϵ��ȷ���ǣ�������
| A��ij��Һ����ˮ�������c��H+��=1��10-amol/L����a��7ʱ������ҺpHһ��Ϊ14-a |
| B��0.1mol/L��KHA��Һ����pH=10��c��K+����c��A2-����c��HA-����c��OH-�� |
| C����0.2mol/L��ijһԪ��HA��Һ��0.1 mol/L NaOH��Һ�������Ϻ���ҺpH����7����Ӧ��Ļ��Һ��c��HA����C��Na+����c��A-�� |
| D��������������ʵ���Ũ�ȵ�Na2CO3��Һ��NaHCO3��Һ��ϣ�3c��Na+��=2c��CO32-��+2c��HCO3-��+2c��H2CO3�� |
