��Ŀ����
 ���Ĺ̶���ָ����Ԫ��������̬ת��Ϊ����̬�Ĺ��̣��ݱ��������¡���ѹ�����������£�N2�ڲ��������������Ķ������Ѵ�����������ˮ������Ӧ�����ɵ���Ҫ����ΪNH3����Ӧ���Ȼ�ѧ����ʽΪ��2N2��g��+6H2O��l��?4NH3��g��+3O2��g����H=+1530.0kJ/mol��Ŀǰ��ҵ�ϳɰ���ԭ���ǣ�N2��g��+3H2��g��?2NH3��g����H=-93.0kJ/mol��
���Ĺ̶���ָ����Ԫ��������̬ת��Ϊ����̬�Ĺ��̣��ݱ��������¡���ѹ�����������£�N2�ڲ��������������Ķ������Ѵ�����������ˮ������Ӧ�����ɵ���Ҫ����ΪNH3����Ӧ���Ȼ�ѧ����ʽΪ��2N2��g��+6H2O��l��?4NH3��g��+3O2��g����H=+1530.0kJ/mol��Ŀǰ��ҵ�ϳɰ���ԭ���ǣ�N2��g��+3H2��g��?2NH3��g����H=-93.0kJ/mol���ش��������⣺
��1��д����ʾ����ȼ���ȵ��Ȼ�ѧ����ʽ
��2���ں��º����ܱ������н��еĹ�ҵ�ϳɰ���Ӧ�������ܱ�ʾ�ﵽƽ��״̬����
A����������ѹǿ���ٷ����仯
B����������ƽ����Է����������ٷ����仯
C���������ʵ�Ũ�ȱ�ǡ�õ��ڻ�ѧ����ʽ�и����ʵĻ�ѧ������֮��
D����λʱ���ڶϿ�3a��H-H����ͬʱ�γ�6a��N-H��
E����Ӧ������N2��NH3�����ʵ����ı�ֵ���ٷ����仯
��3����һ���¶��£����ݻ����䣨ʼ��Ϊ10L�����ܱ������м���2mol N2��8mol H2�����������10���Ӻ�Ӧ�ﵽƽ��״̬������������ѹǿ��Ϊ��ʼ��80%��10�������õ�����Ũ�ȱ�ʾ�Ļ�ѧ��Ӧ����Ϊ
��4��ԭ����H2��ͨ����Ӧ CH4��g��+H2O��g���TCO��g��+3H2��g����ȡ����֪�÷�Ӧ�У�����ʼ������е�
| n(H2O) |
| n(CH4) |
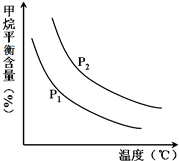
��ͼ�У��������߱�ʾѹǿ�Ĺ�ϵ�ǣ�P1
�ڸ÷�ӦΪ
���㣺�Ȼ�ѧ����ʽ,��ѧƽ���Ӱ������,��ѧƽ��״̬���ж�,����İٷֺ�����Ũ�ȡ�ʱ��ı仯����
ר�⣺��ѧƽ��ר��
��������1����֪��2N2��g��+6H2O��l��?4NH3��g��+3O2��g����H=+1530.0kJ/mol��
��N2��g��+3H2��g��?2NH3��g����H=-93.0kJ/mol�����ø�˹���ɽ�
�ɵ�����ȼ�յ��Ȼ�ѧ����ʽ��
��2���ﵽƽ��ʱ�����淴Ӧ������ȣ������ʵ�Ũ�Ȳ��䣬�Դ�������һЩ������Ҳ���䣬�Դ��ж��Ƿ�ﵽƽ��״̬��
��3����μӷ�Ӧ�ĵ��������ʵ���Ϊamol����������ʽ��ʾ�������ʵı仯����ƽ��ʱ���ʵ���������ѹǿ֮�ȵ������ʵ���֮���з��̼���a�����ݷ�Ӧ���ʸ������V=
��ת����=
��100%��ƽ�ⳣ������������ƽ��Ũ���ݴη��˻����Է�Ӧ��ƽ��Ũ���ݴη��˻�����õ���
��4��������ͼ��仯��������ͬ�¶��£�CH4��g��+H2O ��g���TCO��g��+3H2��g������Ӧ�������������ķ�Ӧ��ѹǿԽ��ƽ��������У�����ƽ�⺬��Խ�ߣ�
��ѹǿһ�����¶����ߣ�����ƽ�⺬����С��ƽ��������У�����ƽ���ƶ�ԭ�������жϣ�
��N2��g��+3H2��g��?2NH3��g����H=-93.0kJ/mol�����ø�˹���ɽ�
| �ڡ�2-�� |
| 6 |
��2���ﵽƽ��ʱ�����淴Ӧ������ȣ������ʵ�Ũ�Ȳ��䣬�Դ�������һЩ������Ҳ���䣬�Դ��ж��Ƿ�ﵽƽ��״̬��
��3����μӷ�Ӧ�ĵ��������ʵ���Ϊamol����������ʽ��ʾ�������ʵı仯����ƽ��ʱ���ʵ���������ѹǿ֮�ȵ������ʵ���֮���з��̼���a�����ݷ�Ӧ���ʸ������V=
| ��c |
| ��t |
| ������ |
| ��ʼ�� |
��4��������ͼ��仯��������ͬ�¶��£�CH4��g��+H2O ��g���TCO��g��+3H2��g������Ӧ�������������ķ�Ӧ��ѹǿԽ��ƽ��������У�����ƽ�⺬��Խ�ߣ�
��ѹǿһ�����¶����ߣ�����ƽ�⺬����С��ƽ��������У�����ƽ���ƶ�ԭ�������жϣ�
���
�⣺��1����֪��2N2��g��+6H2O��l��?4NH3��g��+3O2��g����H=+1530.0kJ/mol��
��N2��g��+3H2��g��?2NH3��g����H=-93.0kJ/mol�����ø�˹���ɽ�
�ɵ�H2��g��+
O2��g��=H2O��l����H=-286.0 kJ/mol��
�ʴ�Ϊ��H2��g��+
O2��g��=H2O��l����H=-286.0 kJ/mol��
��2��A����������ѹǿ���ٷ����仯���ں��º����ܱ������У���Ϊ�ϳɰ������������Ŀ��С�ķ�Ӧ����������ѹǿ���ٷ����仯��˵���ﵽƽ��״̬����A��ȷ��
B����Ӧǰ����������ʵ�������ȣ�����������Է����������ٷ����仯����˵������������ʵ������䣬˵���ﵽƽ��״̬����B��ȷ��
C���������ʵ�Ũ�ȱ�ǡ�õ��ڻ�ѧ����ʽ�и����ʵĻ�ѧ������֮�ȣ��������ʵ�Ũ�ȱ�ǡ�õ��ڻ�ѧ����ʽ�и����ʵĻ�ѧ������֮�ȿ���ֻ��ijһʱ�̵ı�ֵ������֤���Ƿ�ﵽƽ�⣬��C����
D�������Ƿ�ﵽƽ��״̬�������ڵ�λʱ���ڶϿ�3a��H-H����ͬʱ�γ�6a��N-H��������˵���ﵽƽ��״̬����D����
E����Ӧ������N2��NH3�����ʵ����ı�ֵ���ٷ����仯��˵��������Ũ�Ȳ��䣬��Ӧ�ﵽƽ��״̬����E��ȷ��
�ʴ�Ϊ��ABE��
��3����μӷ�Ӧ�ĵ��������ʵ���Ϊamol����
N2��g��+3H2��g���T2NH3��g��
��ʼ��mol����2 8 0
ת����mol����a 3a 2a
ƽ�⣨mol����2-a 8-3a 2a
��2-a+8-3a+2a=��2+8����80%�����a=1
�����ķ�Ӧ����=
=0.01 mol?L-1?min-1��
������ת����=
��100%=50%��
ƽ�ⳣ��K=
=3.2 L2/mol2
�ʴ�Ϊ��0.01 mol?L-1?min-1�� 50%��3.2 L2/mol2
��4��������ͼ��仯��������ͬ�¶��£�CH4��g��+H2O ��g���TCO��g��+3H2��g������Ӧ�������������ķ�Ӧ��ѹǿԽ��ƽ��������У�����ƽ�⺬��Խ�ߣ�����P2��P1���ʴ�Ϊ������
��ѹǿһ�����¶����ߣ�����ƽ�⺬����С��ƽ��������У�����ӦΪ���ȷ�Ӧ���ʴ�Ϊ�����ȣ�
��N2��g��+3H2��g��?2NH3��g����H=-93.0kJ/mol�����ø�˹���ɽ�
| �ڡ�2-�� |
| 6 |
| 1 |
| 2 |
�ʴ�Ϊ��H2��g��+
| 1 |
| 2 |
��2��A����������ѹǿ���ٷ����仯���ں��º����ܱ������У���Ϊ�ϳɰ������������Ŀ��С�ķ�Ӧ����������ѹǿ���ٷ����仯��˵���ﵽƽ��״̬����A��ȷ��
B����Ӧǰ����������ʵ�������ȣ�����������Է����������ٷ����仯����˵������������ʵ������䣬˵���ﵽƽ��״̬����B��ȷ��
C���������ʵ�Ũ�ȱ�ǡ�õ��ڻ�ѧ����ʽ�и����ʵĻ�ѧ������֮�ȣ��������ʵ�Ũ�ȱ�ǡ�õ��ڻ�ѧ����ʽ�и����ʵĻ�ѧ������֮�ȿ���ֻ��ijһʱ�̵ı�ֵ������֤���Ƿ�ﵽƽ�⣬��C����
D�������Ƿ�ﵽƽ��״̬�������ڵ�λʱ���ڶϿ�3a��H-H����ͬʱ�γ�6a��N-H��������˵���ﵽƽ��״̬����D����
E����Ӧ������N2��NH3�����ʵ����ı�ֵ���ٷ����仯��˵��������Ũ�Ȳ��䣬��Ӧ�ﵽƽ��״̬����E��ȷ��
�ʴ�Ϊ��ABE��
��3����μӷ�Ӧ�ĵ��������ʵ���Ϊamol����
N2��g��+3H2��g���T2NH3��g��
��ʼ��mol����2 8 0
ת����mol����a 3a 2a
ƽ�⣨mol����2-a 8-3a 2a
��2-a+8-3a+2a=��2+8����80%�����a=1
�����ķ�Ӧ����=
| ||
| 10min |
������ת����=
| 1mol |
| 2mol |
ƽ�ⳣ��K=
(
| ||||
|
�ʴ�Ϊ��0.01 mol?L-1?min-1�� 50%��3.2 L2/mol2
��4��������ͼ��仯��������ͬ�¶��£�CH4��g��+H2O ��g���TCO��g��+3H2��g������Ӧ�������������ķ�Ӧ��ѹǿԽ��ƽ��������У�����ƽ�⺬��Խ�ߣ�����P2��P1���ʴ�Ϊ������
��ѹǿһ�����¶����ߣ�����ƽ�⺬����С��ƽ��������У�����ӦΪ���ȷ�Ӧ���ʴ�Ϊ�����ȣ�
���������⿼����ۺϣ��漰֪ʶ��϶࣬�漰ͨ��ͼ�������ѧ��Ӧ���ʡ���ѧƽ�⼰���㡢ƽ�ⳣ���ļ���Ӧ���Լ��Ȼ�ѧ����ʽ��˹���ɼ�������⣬��Ҫ��ͼ������жϣ�ƽ���ƶ�ԭ��������Ӧ�ã�Ϊ��Ƶ���㣬������ѧ���ķ��������ͼ��������Ŀ��飬��Ҫѧ����ǿ�Ĺ۲�������˼ά�������Ѷ��еȣ�

��ϰ��ϵ�д�
�����Ŀ
���и����б�����ȷ���ǣ�������
A��F-�Ľṹʾ��ͼ��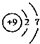 |
B��CO2�ķ���ģ��ʾ��ͼ��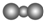 |
C��CSO�ĵ���ʽ��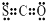 |
| D��N2�Ľṹʽ��N��N�� |
���й��ڽ���Na�������У�˵����ȷ���ǣ�������
| A��Na�ڿ�����ȼ�գ�������ɫ���� |
| B��Na�ڿ�����ȼ�գ�������Na2O |
| C��Na������ɫ������Ӳ�ȴ��۵�� |
| D��Na��K�Ͻ����ԭ�ӷ�Ӧ�ѵĵ��ȼ� |
