题目内容
【题目】下列关于水的电离平衡的相关说法正确的是
A.c(H+)=![]() 的溶液一定呈中性
的溶液一定呈中性
B.将水加热,Kw增大,pH增大,呈碱性
C.向水中加入少量硫酸氢钠固体,溶液的c(H+)增大,平衡逆向移动,Kw减小
D.向0.1 mol·L-1醋酸溶液中加水,溶液中水电离产生的c(H+)将减小
【答案】A
【解析】
A.根据Kw=c(H+)c(OH-),c(H+)=![]() ,说明溶液中c(H+)=c(OH-),溶液一定呈中性,故A正确;
,说明溶液中c(H+)=c(OH-),溶液一定呈中性,故A正确;
B.水的电离是吸热反应,升高温度,促进水电离,溶液中c(H+)增大,pH减小,但水电离出的c(H+)=c(OH-),溶液显中性,故B错误;
C.Kw只与温度有关,向水中加入少量硫酸氢钠固体,溶液的c(H+) 增大,平衡逆向移动,但Kw不变,故C错误;
D.酸电离出来的氢离子能抑制水的电离,向0.1 molL-1醋酸溶液中加水,酸的浓度减小,对水的电离的抑制程度减小,则溶液中水的电离产生的c(H+) 将增大,故D错误;
故选A。

 名校课堂系列答案
名校课堂系列答案【题目】下表是元素周期表的一部分,按要求完成各小题。
IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
2 | ⑥ | ⑦ | ||||||
3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
4 | ② | ④ | ⑨ |
(1)元素①的元素符号:_______________
(2)元素⑧的单质电子式_______________
(3)元素⑤的原子结构示意图______________
(4)化学性质最不活泼的元素______(填元素符号,下同),非金属性最强的元素是________。金属性最强的单质_______。
(5)①③⑤三种元素的最高价氧化物水化物中,碱性最强的 _____(填化学式,下同)。①③⑤三种元素的原子半径由大到小的顺序为_____________。
(6)某元素的最高价氧物的水化物既能与酸反应生成盐和水又能与碱反应生成盐与水,该元素的最高价氧化物和盐酸反应的化学方程式为 _____,与氢氧化钠溶液反应的化学方程式_____。
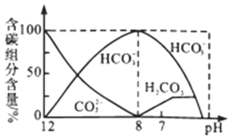
【题目】25℃时,部分物质的电离平衡常数如表所示:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | 10-5 | K1=4×10-7 K2=4×10-11 | 10-8 |
请回答下列问题:
(1)a.CH3COOH、b.H2CO3、c.HClO的酸性由强到弱的顺序为___。(填字母)
(2)物质的量浓度均为0.1mol/L的四种溶液:
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
pH由小到大排列的顺序是___(填字母)
(3)常温下0.1mol/LCH3COOH溶液加水稀释过程中,下列各项中数值变大的是___(填字母)
A.c(H+) B.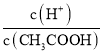 C.c(H+)·c(OH-)
C.c(H+)·c(OH-)
D.![]() E.
E.![]() F.
F.![]()
(4)25℃时,H2SO3![]() HSO3-+H+的电离常数Ka=1×10-2mol/L,则该温度下pH=3、c(HSO3-)=0.1mol/L的NaHSO3溶液中c(H2SO3)=___。
HSO3-+H+的电离常数Ka=1×10-2mol/L,则该温度下pH=3、c(HSO3-)=0.1mol/L的NaHSO3溶液中c(H2SO3)=___。
【题目】下列实验操作、现象与实验解释或结论正确的是![]()
![]()
编号 | 实验操作和现象 | 实验解释或结论 |
A | 向工业酒精中加入一小块钠,产生气泡 | 乙醇中含有羟基 |
B | 向锌和稀硫酸反应液中滴加几滴CuSO4溶液,速率加快 | CuSO4溶液起到了催化剂的作用 |
C | 将AlCl3熔化,没能检测到导电性 | AlCl3不是离子化合物 |
D | 将一定量的油脂加入到稀硫酸中,加入一段时间后静置,混合液仍分层 | 油脂在酸性条件下不能发生水解反应 |
A.AB.BC.CD.D