题目内容
【题目】常温下,向20mL![]()
![]()
![]() 溶液中逐滴加入
溶液中逐滴加入![]()
![]() HCl溶液40mL,溶液中含碳元素的各种微粒
HCl溶液40mL,溶液中含碳元素的各种微粒![]() 逸出未画出
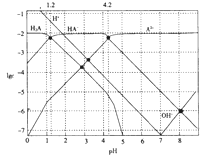
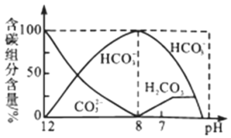
逸出未画出![]() 的物质的量分数随溶液pH变化的部分情况如图所示,下列说法错误的是
的物质的量分数随溶液pH变化的部分情况如图所示,下列说法错误的是![]()
A.在同一溶液中,![]() 、
、![]() 、
、![]() 不能大量共存
不能大量共存
B.已知在![]() ,
,![]() 的水解平衡常数
的水解平衡常数![]() ,当溶液的
,当溶液的![]() 时,溶液中
时,溶液中![]() :
:![]() :1
:1
C.![]() 时溶液中各种离子其物质的量浓度的大小关系是
时溶液中各种离子其物质的量浓度的大小关系是![]()
D.当混合液![]() 时,开始放出
时,开始放出![]() 气体
气体
【答案】C
【解析】
根据题意可知,本题考查离子浓度的比较,运用碳酸钠与盐酸的反应及图象分析。
![]() 由图可知,pH在
由图可知,pH在![]() 存在
存在![]() 、
、![]() ,
,![]() 存在
存在![]() 、
、![]() ,可知上述反应的同一溶液中,
,可知上述反应的同一溶液中,![]() 、
、![]() 、
、![]() 不能大量共存,故A正确;
不能大量共存,故A正确;
B.![]() 的水解平衡常数
的水解平衡常数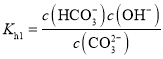 ,当溶液的
,当溶液的![]() 时,
时, ![]() ,
,![]() ,则溶液中
,则溶液中![]() :
:![]() :1,故B正确;
:1,故B正确;
C.由图可知![]() 时
时![]() ,
,![]() ,且溶液含
,且溶液含![]() ,则溶质为NaCl、
,则溶质为NaCl、![]() 、
、![]() ,则存在
,则存在![]() ,故C错误;
,故C错误;
D.由图可知,![]() 时溶液含
时溶液含![]() ,此时碳酸根已经几乎没有了,那么,
,此时碳酸根已经几乎没有了,那么,![]() 与
与![]() 分数之和应该接近于1,从图像看,当pH约为6时,碳酸含量几乎不再变化,
分数之和应该接近于1,从图像看,当pH约为6时,碳酸含量几乎不再变化,![]() 与
与![]() 分数之和小于1,说明碳酸已经达到饱和,若酸性再增强,将释放二氧化碳;因此说混合液
分数之和小于1,说明碳酸已经达到饱和,若酸性再增强,将释放二氧化碳;因此说混合液![]() 时,开始放出
时,开始放出![]() 气体,故D正确;
气体,故D正确;
答案选C。

练习册系列答案
 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目