��Ŀ����
18�� ��������泥�NH2COONH4����һ�ְ�ɫ���壬�ֽ⡢��ˮ�⣬���������ϡ�������ϴ�Ӽ��ȣ�ʵ�����Ʊ���������泥�NH2COONH4���ķ�Ӧ���£�
��������泥�NH2COONH4����һ�ְ�ɫ���壬�ֽ⡢��ˮ�⣬���������ϡ�������ϴ�Ӽ��ȣ�ʵ�����Ʊ���������泥�NH2COONH4���ķ�Ӧ���£�2NH3��g��+CO2��g��?NH2COONH4��s����H��0
����Ӧ�У�NH2COONH4+H2O?NH4HCO3+NH3���� NH2COONH4��s��$\stackrel{��}{?}$2NH3��g��+CO2��g���ȣ�
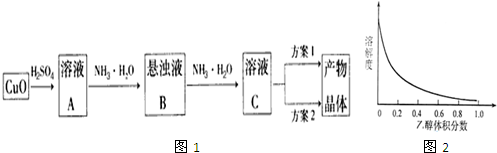
��֪����İ����Ͷ�����̼����ͨ��������ȴ�ķ�Ӧ��ʱ���������ϻ��γ�һ�����ܡ���Ӳ��ճ������ǿ�İ�������泥���㲻�������ﲻ��Ӱ��ɢ�ȣ�����Ҳʹ���ﲻ��ȡ������ˣ���ʵ���ҵ���Ҫʵ��װ�úͲ�����ͼ1��
ע�����Ȼ�̼��Һ��ʯ����Ϊ���Խ��ʣ�
��I���ϳɣ��Ѱ����Ͷ�����̼ͨ�����Ȼ�̼�У����Ͻ����ϣ����ɵİ��������ϸС�������������Ȼ�̼�У� ��������϶�ʱ��ֹͣ�Ʊ���
���������ᴿ������������林����Ȼ�̼�з��룬�ؽᾧ�ᴿ��
����Ʒ���ȷ���
�ش��������⣺
��1������a�����ƣ�ˮ�ۣ�Һ��ʯ������ƿ��������ͨ���۲����ݣ�����NH3��CO2ͨ�������
��2������ͼ2װ����ȡƽ�ȵ�CO2����������ѡ����Լ���ʯ��ʯ��ϡ���ᣨ��ϡ���ᣩ��
����װ�������Եķ����ǹرշ�Һ©����������������ˮ�У����֣�����ë������ס��ƿ�����ܿ������ݣ����ֺ��γ�ˮ���Ҳ��½���˵����©ˮ
��3���ϳɹ�����ʹ�������Ȼ�̼�����õ綯���������Ͻ��裬������ʹ�����Ȼ�̼��Ϊ��ɢ����������Ϊ��ʹNH3��CO2��ֽӴ�������������������ϵ�ճ����
��4���������ñ�ˮ��ȴ��ԭ���ǽ����¶ȣ���߷�Ӧ��ת���ʣ����¶ȣ���ֹ��Ӧ������ɲ���ֽ⣩��
��5���ӷ�Ӧ��Ļ�����з������Ʒ���õ������Ʒ��ʵ�鷽����C
A�� ���˺�ѹ���Ⱥ�� ��B�����˺�ѹ���Ⱥ��
C�����˺����40�����º�ɡ�����D�����˺����40�����º��
��6��β������װ����ͼ3��ʾ��˫ͨ�����ܵ����ã���ֹ������Ũ��������ã����ն��ఱ������ֹ������ˮ�������뷴Ӧ��ʹ���������ˮ�⣮
��7��ȡ�ֱ��ʶ�����̼����淋İ����������Ʒ0.7820g��������ʯ��ˮ��ִ�����ʹ̼Ԫ����ȫת��Ϊ̼��ƣ����ˡ�ϴ�ӡ�����������Ϊ1.000g������Ʒ�а�������淋����ʵ�������Ϊ80%��
���� ��1��ˮ��������ˮ���ռ����壬������ʢ�Ŵ���Һ�壬����aΪˮ�ۣ�Һ��ʯ������ƿ����Ҫ�����ǿ��Ʒ�Ӧ���г̶ȣ������������ٺ�ԭ���������ȣ�
��2��������̼��ʵ�����Ʒ�����ϡ�����ϡ���������ʯ��Ӧ�����������ᣬ�������̼��Ʒ�Ӧ�������������ֹ��Ӧ��һ�����У�װ�������Լ����ԭ���ǣ�ͨ�����巢�����븽���Һ�幹�ɷ����ϵ�����ݸı���ϵ��ѹǿʱ���������������ݵ����ɡ�ˮ�����γɡ�Һ��������ȣ����ж�װ�������Եĺû���
��3���ϳɹ�����ʹ�������Ȼ�̼�����Ȼ�̼Ϊ��ɢ����������Ϊ��ʹNH3��CO2��ֽӴ�������������������ϵ�ճ����
��4����Ӧ�Ƿ��ȷ�Ӧ������ƽ��������У�
��5�����ɵİ��������С�������������Ȼ�̼�У������Ʒ��ʵ�鷽�����ù��˵õ�����������泥�NH2COONH4����һ�ְ�ɫ���壬�ֽ⣻
��6�����ݷ�Ӧ�����еIJ�����������ܰ���Ⱦ�Ե������ŷŵ������У�����������ˮ��������Ҫ�ŵ�����
��7��̼����淋İ����������Ʒ�У�ʹ̼Ԫ����ȫת��Ϊ̼��ƣ�����̼Ԫ���غ�ͻ���������������ʵ�����������
��� �⣺��1������a�����ƣ�ˮ������ʢ�Ŵ���Һ���ˮ��Һ��ʯ������ƿ�������ǿ��Ʒ�Ӧ���г̶ȣ������������ٺ�ԭ���������ȣ�
�ʴ�Ϊ��ˮ�ۣ�ͨ���۲����ݣ�����NH3��CO2ͨ�������
��2��������̼��ʵ�����Ʒ�����ϡ���������ʯ��Ӧ����Ӧ�Ļ�ѧ����ʽΪ��CaCO3+2HCl�TCaCl2+CO2��+H2O������ϡ����CaCO3+2HNO3�TCa��NO3��2+CO2��+H2O������װ�������Եķ������رշ�Һ©����������������ˮ�У����֣�����ë������ס��ƿ�����ܿ������ݣ����ֺ��γ�ˮ���Ҳ��½���˵����©ˮ��
�ʴ�Ϊ��ʯ��ʯ��ϡ���ᣨ��ϡ���ᣩ���رշ�Һ©����������������ˮ�У����֣�����ë������ס��ƿ�����ܿ������ݣ����ֺ��γ�ˮ���Ҳ��½���˵����©ˮ��
��3����������淋�ճ������ǿ���������ϲ���Ӱ��ɢ�ȣ�����Ҳʹ���ﲻ��ȡ����ʹ�����Ȼ�̼��Ϊ��ɢ����������Ϊ��ʹNH3��CO2��ֽӴ�������������������ϵ�ճ����
�ʴ�Ϊ��ʹ�����Ȼ�̼��Ϊ��ɢ����������Ϊ��ʹNH3��CO2��ֽӴ�������������������ϵ�ճ����
��4����Ӧ2NH3��g��+CO2��g��?NH2COONH4��s��+Q���Ƿ��ȷ�Ӧ������ƽ��������У��¶����ߣ��������ñ�ˮ��ȴ��߷�Ӧ����ת���ʣ���ֹ�������¶ȹ��߷ֽ⣬
�ʴ�Ϊ�������¶ȣ���߷�Ӧ��ת���ʣ����¶ȣ���ֹ��Ӧ������ɲ���ֽ⣩��
��5���Ʊ���������淋�װ����ͼ3��ʾ���Ѱ����Ͷ�����̼ͨ�����Ȼ�̼�У����Ͻ����ϣ����ɵİ��������С�������������Ȼ�̼�У������Ʒ��ʵ�鷽�����ù��˵õ�����������泥�NH2COONH4����һ�ְ�ɫ���壬�ֽ⡢���ܼ��Ⱥ�ɣ�Ӧ�����40�����º�ɣ�
�ʴ𰸣�C��
��6��˫ͨ�����ܵ������Ƿ�ֹҺ�嵹����Ũ���������ն���İ�����ͬʱ��ֹ������ˮ�������뷴Ӧ��ʹ���������ˮ�⣬
�ʴ�Ϊ����ֹ���������ն��ఱ������ֹ������ˮ�������뷴Ӧ��ʹ���������ˮ�⣻
��7��ȡ�ֱ��ʶ�����̼����淋İ����������Ʒ0.782g��������ʯ��ˮ��ִ�����ʹ̼Ԫ����ȫת��Ϊ̼��ƣ����ˡ�ϴ�ӡ�����������Ϊ1.000g�����ʵ���Ϊ$\frac{1.000g}{100g/mol}$=0.01mol������Ʒ�а�����������ʵ���Ϊx��̼��������ʵ���Ϊy����̼Ԫ���غ��֪��
x+y=0.01
78x+79y=0.782
���x=0.008mol
y=0.002mol
����Ʒ�а�������淋���������=$\frac{0.008mol��78g/mol}{0.782g}$��100%��80%��
�ʴ�Ϊ��80%��
���� ���⿼���������Ʊ�ʵ������Ӧ�ã���Ҫ�ǰ������Ʊ�����������������Ʊ�ʵ��װ�÷����жϣ�ʵ��������������������ʵ����ƣ��йػ����ļ��㣬��Ŀ�Ѷ��еȣ�

 ȫ�ſ��䵥Ԫ�����������ܸ�ϰϵ�д�
ȫ�ſ��䵥Ԫ�����������ܸ�ϰϵ�д�| ��� | H2SO4 | Na2S2O3 | H2O��ml�� |
| A | 5ml 0.1mol/L | 5ml 0.1mol/L | 0 |
| B | 5ml 0.2mol/L | 5ml 0.1mol/L | 10 |
| C | 5ml 0.3mol/L | 5ml 0.1mol/L | 20 |
| D | 5ml 0.4mol/L | 5ml 0.1mol/L | 30 |
| A�� | A | B�� | B | C�� | C | D�� | D |
| A�� | H2O��H2S��H2Se | B�� | Hg��Na��NaCl | ||
| C�� | ����衢���ʯ��̼���� | D�� | S��Br2��O3 |
��1�����÷�ӦCa��s��+O2$\frac{\underline{\;\;��\;\;}}{\;}$CaO2��s�����ڴ��������£���ȡCaO2��װ��ʾ��ͼ1���£�
��ش��������⣺
��װ��A�з�Ӧ�Ļ�ѧ����ʽΪ2H2O2$\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2��������a������Ϊ������ƿ��
װ��D��ʢ�е�Һ����Ũ���ᣬ������һ�ǹ۲����������٣��ж�����ͨ���Ƿ���켰������Ʒ�Ӧ���еij̶ȣ����Ƿ�ֹ��������Cװ��Ӱ���Ʒ���ȣ�������װ��Ӧ���е�ʵ�������
a��ͨ������ b�����װ�������� c������ҩƷ d��ֹͣͨ����
e����ȼ�ƾ��� f��Ϩ��ƾ��� g����ȴ�����£�
��ȷ�IJ���˳��Ϊbcaefgd��
����ȫ��Ӧ���й����ݼ�¼���£�
| �մ�������m0/g | ������Ƶ�����m1/g | ��������������m2/g |
| 14.80 | 15.08 | 15.25 |
��2�����÷�ӦCa2++H2O2+2NH3•H2O+6H2O=CaO2•8H2O+2NH4+���ڼ��Ի����У���ȡCaO2������ʾ��ͼ2���£�
��ش��������⣺
������Ӧ�У�NH3•H2O��Ca2+��H2O2�ķ�Ӧ������������������к��������Ca2+��Ӧ�����������ӣ��ٽ���Ӧ���У��÷�Ӧ���������������Ϊacf������ĸ����
a�����Ȼ�����Һ��μ����������-��ˮ��Һ��
b���ѹ�������-��ˮ��Һ��μ����Ȼ�����Һ��
c���μ�ʱ�Ƚ�����ã��۲쾧������
d���μ�ʱ��ͣ���裬ֱ��������ȫ����
e����Ӧ��ϵ��ˮԡ����
f����Ӧ��ϵ��ˮԡ��ȴ
ϴ��CaO2•8H2O����ʱ���жϾ����Ƿ���ȫϴ�����Լ�ΪAgNO3��Һ����Һѭ��ʹ��ʱ���ڷ�Ӧ���м���һ�����ʣ������ʵĻ�ѧʽΪCa��OH��2��
�����÷�Ӧ2CaO2 ��350��?2CaO+O2��������Ʒ��CaO2����ʱ��ֹͣ��Ӧ����ȴ��25����װ��ʾ��ͼ3���£���ֱ�Ӷ���ȷ��25�桢1����ѹ��������������������ƫ���ƫ����ƫС������Ӱ�족����

 ��1����ѧƽ�ⳣ��K��ʾ���淴Ӧ�Ľ��г̶ȣ�KֵԽ��ʾ���淴Ӧ���еij̶�Խ��Kֵ��С���¶ȵĹ�ϵ�ǣ��¶����ߣ�Kֵ��ȷ�����������С������ȷ��������
��1����ѧƽ�ⳣ��K��ʾ���淴Ӧ�Ľ��г̶ȣ�KֵԽ��ʾ���淴Ӧ���еij̶�Խ��Kֵ��С���¶ȵĹ�ϵ�ǣ��¶����ߣ�Kֵ��ȷ�����������С������ȷ����������2����һ���Ϊ10L�������У�ͨ��һ������CO��H2O����850��ʱ�������·�Ӧ��CO��g��+H2O��g��?CO2��g��+H2��g����H=-QkJ/mol ��Q��0����CO��H2OŨ�ȱ仯��ͼ��
T��ʱ����Ũ�ȣ�mol•L-1���ı仯��
| ʱ�䣨min�� | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
�ٱ���c1��ֵ����0.08mol/L ������ڡ�С�ڻ���ڣ���
�ڷ�Ӧ��4min��5min֮�䣬ƽ�����淽���ƶ������ܵ�ԭ����d������5min��6min֮����ֵ�����仯�����ܵ�ԭ����a��
a������ˮ���� b�������¶� c��ʹ�ô��� d����������Ũ��
��3������T��ʱ���ܱ������д������·�Ӧ��2SO2 ��g��+O2��g��?2SO3��g����H��0��
��֪����Ӧ��ʼʱc��SO2��=0.4mol/L��c��O2��=1mol/L�����ⶨ�÷�Ӧ�ڸ��¶��µ�ƽ�ⳣ��K��19�����жϣ�����Ӧ���е�SO2ת����Ϊ50%ʱ���÷�Ӧ�Ƿ�ﵽƽ��״̬δ��ƽ�⣨�ƽ��״̬����δ��ƽ�⡱������������ΪŨ����Qc=1.1��19������δ�ﵽƽ�⣻��δ�ﵽƽ��״̬���÷�Ӧ��ʱ����������У������������
| A�� | ʯī������ʯ�ȶ� | |
| B�� | ���ʯ��ʯīһ���ȶ� | |
| C�� | �������Ľ��ʯ��ʯī��ȫȼ�գ��ų�������һ���� | |
| D�� | �������Ľ��ʯ��ʯī��ȫȼ�գ�ʯī�ų��������� |
| A�� | 10s | B�� | ����10s | C�� | С��10s | D�� | ���ж� |
| A�� | �¶� | B�� | ѹǿ | C�� | ��Ӧ�ﱾ������ | D�� | ���� |