题目内容
【题目】某温度下,向10 mL 0.1 mol/L CuCl2溶液中滴加0.1mol/L的Na2S溶液,滴加过程中-lg c(Cu2+)与Na2S溶液体积的关系如图所示.下列有关说法正确的是( )

A.向10 mL Ag+、Cu2+物质的量浓度均为0.1mol/L的混合溶液中逐滴加入0.01mol/L的Na2S溶液,Cu2+先沉淀[已知:Ksp(Ag2S)=6.4×10-50]
B.0.1mol/LNa2S溶液中:c(OH-)=c(H+)+c(HS-)+c(H2S)
C.a、b、c三点对应的溶液中,水的电离程度最大的为b点
D.该温度下,Ksp(CuS)的数量级为10-36
【答案】D
【解析】
A、刚开始产生Ag2S沉淀时,c2(Ag+)×c(S2-)=Ksp(Ag2S),其中c(Ag+)=0.1mol·L-1,则此时c(S2-)=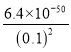 mol·L-1=6.4×10-48mol·L-1,同理,刚产生刚开始产生CuS沉淀时,c (Cu2+)×c(S2-)=Ksp(CuS),其中c(Cu2+)=0.1mol·L-1,则此时c(S2-)=
mol·L-1=6.4×10-48mol·L-1,同理,刚产生刚开始产生CuS沉淀时,c (Cu2+)×c(S2-)=Ksp(CuS),其中c(Cu2+)=0.1mol·L-1,则此时c(S2-)=![]() mol·L-1=10-34.4mol·L-1,所以Ag+先沉淀,故A错误;
mol·L-1=10-34.4mol·L-1,所以Ag+先沉淀,故A错误;
B、Na2S溶液中质子守恒关系为c(OH-)=c(H+)+c(HS-)+2c(H2S),故B错误;
C、a、c两点Cu2+、S2-的水解促进了水的电离,水的电离程度增大,b点可认为是NaCl溶液,水的电离没有被促进,水的电离程度最小,故C错误;
D、b点CuCl2和Na2S溶液恰好反应生成CuS沉淀,即为CuS的饱和溶液,溶液中c(S2-)=c(Cu2+)=10-17.7,Ksp(CuS)=c(S2-)×c(Cu2+)=10-17.7×10-17.7=10-35.4=100.6×10-36,即Ksp(CuS)数量级为10-36,故D正确;
故选D。

 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案




