题目内容
【题目】设![]() 为阿伏加德罗常数值,下列说法正确的是( )
为阿伏加德罗常数值,下列说法正确的是( )
A.![]()
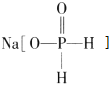
![]() 含有6mol共价键
含有6mol共价键
B.![]() 溶液加热后,溶液的pH减小
溶液加热后,溶液的pH减小
C.常温常压下,![]()
![]() 中含有的分子数为
中含有的分子数为![]() 个
个
D.稀释![]() 溶液,
溶液,![]() 电离程度增大,溶液的导电能力增强
电离程度增大,溶液的导电能力增强
【答案】A
【解析】
根据题中![]() 为阿伏加德罗常数可知,本题考查
为阿伏加德罗常数可知,本题考查![]() 为阿伏加德罗常数的相关计算,运用物质的量的相关计算公式分析。
为阿伏加德罗常数的相关计算,运用物质的量的相关计算公式分析。
A.白磷中含6条![]() 键,故1mol白磷中含6mol共价键,故A正确;
键,故1mol白磷中含6mol共价键,故A正确;
B.盐类水解吸热,故![]() 溶液加热后,其水解程度增大,碱性增强,故溶液的pH增大,故B错误;
溶液加热后,其水解程度增大,碱性增强,故溶液的pH增大,故B错误;
C.常温常压下,气体摩尔体积大于![]() ,故
,故![]() 氯气的物质的量小于1mol,则分子数小于
氯气的物质的量小于1mol,则分子数小于![]() 个,故C错误;
个,故C错误;
D.加水稀释,弱电解质的电离平衡右移,故醋酸的电离程度增大,但由于溶液体积增大,故溶液中离子浓度减小,则导电能力减弱,故D错误;
答案选A。

【题目】某化学兴趣小组对加碘食盐中碘酸钾进行研究,查阅资料得知:碘酸钾是一种白色粉末,常温下很稳定,加热至560℃开始分解。在酸性条件下碘酸钾是一种较强的氧化剂与HI、H2O2等物质作用,被还原为单质碘。
(1)学生甲设计实验测出加碘食盐中碘元素的含量,步骤如下:
①称取wg加碘盐,加适量蒸馏水溶解。
②用稀硫酸酸化所得的溶液,再加入过量KI溶液,写出该步反应的离子方程式:_______。
③以淀粉为指示剂,用物质的量浓度为1.00×10-3molL-1的Na2S2O3溶液滴定![]() 滴定时的反应方程式为
滴定时的反应方程式为![]() ,滴定时Na2S2O3溶液应放在 ______
,滴定时Na2S2O3溶液应放在 ______ ![]() 填“酸式滴定管”或“碱式滴定管”
填“酸式滴定管”或“碱式滴定管”![]() ,滴定至终点的现象为_______________。
,滴定至终点的现象为_______________。
(2)学生乙对纯净的NaCl(不含KIO3)进行了下列实验:
顺序 | 步骤 | 实验现象 |
① | 取少量纯净的NaCl,加适量蒸馏水溶解 | 溶液无变化 |
② | 滴入少量淀粉-KI溶液,振荡 | 溶液无变化 |
③ | 然后再滴加稀硫酸,振荡 | 溶液变蓝色 |
请推测实验③中产生蓝色现象的可能原因: __________________ ;根据学生乙的实验结果可推测学生甲的实验结果可能 ______ (填“偏大”、“偏小”或“无影响”)。
(3)学生丙设计实验证明加碘食盐样品中碘元素的存在形式是IO3-而不是I-,进行如下实验。写出实验步骤、预期现象和结论。限选试剂:稀硫酸、稀硝酸、3% H2O2溶液、新制氯水、1%淀粉溶液、蒸馏水。
实验步骤 | 预期现象和结论 |
步骤1:取少量食盐样品于试管中,加适量蒸馏水使其完全溶解, _____________________ | ______ |
步骤2:另取少量食盐样品于试管中,加适量蒸馏水使其完全溶解,滴入适量的稀硫酸酸化, _____________________ | ______ |
【题目】与化学平衡类似,电离平衡的平衡常数,叫做电离常数(用K表示)。下表是某温度下几种常见弱酸的电离平衡常数:
酸 | 电离方程式 | 电离平衡常数K |
CH3COOH | CH3COOH | 2×10-5 |
HClO | HClO | 3.0×10-8 |
H2CO3 | H2CO3 HCO3- | K1=4.4×10-7 K2=5.6×10-11 |
H3PO4 | H3PO4 H2PO4- HPO42- | K1=7.1×10-3 K2=6.3×10-8 K3=4.2×10-13 |
回答下列问题:
(1)若把CH3COOH、HClO、H2CO3、HCO3-、H3PO4、H2PO4-、HPO42-都看作是酸,则它们酸性最强的是___________(填化学式)。
(2)向NaClO溶液中通入少量的二氧化碳,发生的离子方程式为________。
(3)该温度下0.1mol/L的CH3COOH溶液加水稀释过程,下列表达式的数据一定增大的是__。
A c(H+) B c(H+)c(CH3COO![]()
(4)取等体积的pH均为a的醋酸和次氯酸两溶液,分别用等浓度的NaOH稀溶液恰好中和,消耗的NaOH溶液的体积分别为V1,V2,则大小关系为:V1_________V2(填“>”、“<”或“=”)。
(5)下列四种离子结合H+能力最强的是________。
A HCO3- B CO32- C ClO- D CH3COO-
(6)等物质的量的苛性钠分别用pH为2和3的醋酸溶液中和,设消耗醋酸溶液的体积依次为Va、Vb,则两者的关系正确的是_________。
A Va>10Vb B Va<10Vb C Vb<10Va D Vb>10Va
(7)已知100℃时,水的离子积常数Kw=1.0×10-12,pH=3的CH3COOH和pH=9的NaOH溶液等体积混合,混合溶液呈_____________性;
(8)等浓度的①(NH4)2SO4、②NH4HSO4、③NH4HCO3、④NH4Cl、⑤NH3H2O溶液中,NH4+浓度由大到小的顺序是:_________。
(9)计算该温度下CH3COONa的水解平衡常数Kh_________。
(10)物质的量浓度相同的四种溶液:a CH3COONa、b NaHCO3、c NaClO、d Na2CO3
四种溶液的pH由小到大排列的顺序是____________(用编号填写)。
【题目】已知:H2(g)+I2(g)![]() 2HI(g);ΔH= -14.9kJ·mol-1。某温度下在甲、乙两个恒容密闭容器中充入反应物,其起始浓度如下表所示。甲中反应达到平衡时,测得c(H2)=0.008mol·L-1。下列判断正确的
2HI(g);ΔH= -14.9kJ·mol-1。某温度下在甲、乙两个恒容密闭容器中充入反应物,其起始浓度如下表所示。甲中反应达到平衡时,测得c(H2)=0.008mol·L-1。下列判断正确的
起始浓度 | c(H2)/(mol·L-1) | c(I2)/(mol·L-1) | c(HI)(mol·L-1) |
甲 | 0.01 | 0.01 | 0 |
乙 | 0.02 | 0.02 | 0 |
A.平衡时,乙中H2的转化率是甲中的2倍
B.平衡时,甲中混合物的颜色比乙中深
C.平衡时,甲、乙中热量的变化值相等
D.该温度下,反应的平衡常数K=0.25