题目内容
【题目】某溶液中可能含有K+、Na+、Fe3+、Fe2+、SO42-、CO32-、I-、Cl-中的一种或多种,进行如图所示的实验,下列说法正确的是 ( )
A. 溶液X中有Fe3+、SO42-
B. 溶液X中有Fe2+、I-可能有SO42-、Cl-
C. 溶液X中有I-、Cl-,无CO32-
D. 溶液X中有I-,Fe2+和Fe3+两种离子中至少有一种
【答案】B
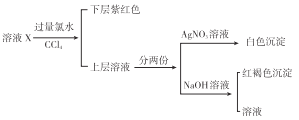
【解析】过量氯水反应后的溶液,加入CCl4萃取后下层的紫红色,说明原溶液中含有I-,则能够氧化I-的Fe3+不能同时存在于溶液中。此时上层的水溶液中一定含有氯水还原生成的Cl-,所以用该溶液加入AgNO3生成的白色沉淀,其中Cl-不能说明存在于原溶液中。另外一份加入NaOH产生红褐色沉淀说明溶液中存在Fe3+,但是该Fe3+又不能存在于原溶液中,那只能是Fe2+开始时被氯水氧化生成Fe3+ ,所以原溶液中含有Fe2+。Fe2+的存在说明原溶液中不含有CO32-。综上所述,原溶液中含有I-、Fe2+,一定不存在Fe3+、CO32-,其他离子不能确定。正确答案B。

练习册系列答案
相关题目





