��Ŀ����
����Ŀ����80��ʱ��0.40mol��N2O4�������2L�Ѿ���յĹ̶��ݻ����ܱ������з������·�Ӧ��N2O4![]() 2NO2��Q����һ��ʱ��Ը������ڵ����ʽ��з������õ��������ݣ�
2NO2��Q����һ��ʱ��Ը������ڵ����ʽ��з������õ��������ݣ�
ʱ�䣨s��n��mol�� | 0 | 20 | 40 | 60 | 80 | 100 |
n��N2O4�� | 0.40 | a | 0.20 | c | d | e |
n��NO2�� | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
��1������20s��40s����N2O4��ʾ��ƽ����Ӧ����Ϊ____��
��2���÷�Ӧ��ƽ�ⳣ��K=___��
��3����Ӧ������100s��Ӧ�������¶Ƚ��ͣ�����������ɫ___��������dz��������������������������
��4��Ҫ����÷�Ӧ��Kֵ���ɲ�ȡ�Ĵ�ʩ�У�����ţ�___����Ҫ���´ﵽƽ��ʱ��ʹ[NO2]/[N2O4]ֵ��С���ɲ�ȡ�Ĵ�ʩ�У�����ţ�___��
A������N2O4����ʼŨ�� B������������ͨ��NO2
C��ʹ�ø�Ч���� D�������¶�
��5����ͼ��80��ʱ������N2O4���ʵ����ı仯���ߣ����ڸ�ͼ�в������÷�Ӧ��60��ʱN2O4���ʵ����ı仯���ߡ�____
���𰸡�![]() 1.8 ��dz D A
1.8 ��dz D A 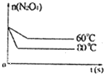
��������
��1���ȸ��ݶ����������ʵ������㷴Ӧ�����������������ʵ����������ʵ�����ȥ��Ӧ�����ʵ�������������ʣ������������������ʵ������ٸ��ݹ�ʽ![]() ����������������ƽ����Ӧ���ʣ�
����������������ƽ����Ӧ���ʣ�
��2������K=![]() ����ƽ�ⳣ����
����ƽ�ⳣ����
��3�������¶�ƽ������ȷ����ƶ�������ƽ���ƶ������ж�������ɫ�仯��
��4����ѧƽ�ⳣ��ֻ���¶��йأ����������ƽ���Ӱ��Ч������
��5�������¶ȣ���ѧ��Ӧ���ʼ�С��ƽ������ȷ����ƶ���
��1����![]() ʱ�����ɶ�������
ʱ�����ɶ�������![]() ������������������
������������������![]() �������л�ʣ��
�������л�ʣ��![]() ����20s��40s����N2O4��ʾ��ƽ����Ӧ����Ϊ
����20s��40s����N2O4��ʾ��ƽ����Ӧ����Ϊ![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��
��2��������![]() ʱ���������������ʵ������ٱ仯�����Է�Ӧ�ﵽƽ��״̬���������������ʵ�����
ʱ���������������ʵ������ٱ仯�����Է�Ӧ�ﵽƽ��״̬���������������ʵ�����![]() �����������������������ʵ�����
�����������������������ʵ�����![]() ����ʣ��
����ʣ��![]() ����
����![]() ��
��
����������ƽ��Ũ��![]() ��������������ƽ��Ũ��
��������������ƽ��Ũ��![]() ��
��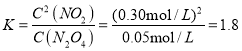 ���ʴ�Ϊ��1.8��
���ʴ�Ϊ��1.8��
��3���÷�Ӧ������Ӧ�����ȷ�Ӧ�������¶ȣ�ƽ�����淴Ӧ�����ƶ������������ĺ������٣����Ի���������ɫ��dz���ʴ�Ϊ����dz
��4����ѧƽ�ⳣ��ֻ���¶��йأ��������κ��������أ�D����ȷ������ѡ��������⣻
A. ����N2O4����ʼŨ�ȣ��൱�ڼ�ѹ����ʹƽ���������ƶ���ʹ[NO2]/[N2O4]ֵ��С��A����ȷ��
B������������ͨ��NO2���൱�ڼ�ѹ����ʹƽ���������ƶ�����NO2���ʵ�������������ʹ��[NO2]/[N2O4]ֵ���B�����
C. ʹ�ø�Ч������ƽ�ⲻ�Զ��ϣ�����ı�[NO2]/[N2O4]ֵ��C�����
D. ��ӦN2O4![]() 2NO2��Q��֪�������¶ȣ�ƽ���������ƶ���[NO2]/[N2O4]ֵ���D�����
2NO2��Q��֪�������¶ȣ�ƽ���������ƶ���[NO2]/[N2O4]ֵ���D�����
��ΪA��
�ʴ�Ϊ��D��A��
��5���������¶ȣ���ѧ��Ӧ���ʼ�С������ƽ������ʱ������ƽ�����淴Ӧ�����ƶ������Ե�����ƽ��ʱ���������������ʵ����ȵ�һ��ƽ��ʱ�٣���![]() ����Ϊ
����Ϊ
 ��
��

����Ŀ����1���ڸ�����һ����̼�ɽ���������ԭΪ������
��֪����C(s)��O2(g)===CO2(g)����H1����393.5 kJ��mol��1
��CO2(g)��C(s)===2CO(g)����H2����172.5 kJ��mol��1
��S(s)��O2(g)===SO2(g)����H3����296.0 kJ��mol��1
��д��CO��SO2��Ӧ���Ȼ�ѧ����ʽ__________________________
��2����2 L�̶�������ܱ������ڣ�800��ʱ��Ӧ2NO(g)��O2(g) ![]() 2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯�����
2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯�����
ʱ��(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
��д���÷�Ӧ��ƽ�ⳣ������ʽ��K��_______________________����֪��K300��>K350������÷�Ӧ��______��Ӧ������ȡ������ȡ�����
����ͼ��ʾNO2�ı仯��������__________����O2��ʾ��0��2 s�ڸ÷�Ӧ��ƽ������v��__________��

����˵���÷�Ӧ�Ѵﵽƽ��״̬����________��
a��v(NO2)��2v(O2) b��������ѹǿ���ֲ���
c��v��(NO)��2v��(O2) d���������ܶȱ��ֲ���
��Ϊʹ�÷�Ӧ�ķ�Ӧ����������ƽ��������Ӧ�����ƶ�����________��
a����ʱ�����NO2���� b���ʵ������¶�
c������O2��Ũ�� d��ѡ���Ч����


