题目内容
氮及其化合物在工农业生产、生活中有着重要作用。
(1)在T℃时,将0.6molH2和0.4molN2置于容积为2 L的密闭容器中(压强为mPa)发生反应:3H2+N2 2NH3 △H<0。若保持温度不变,某兴趣小组同学测得反应过程中容器内压强随时间变化如图所示:8 min内分钟NH3的平均生成速率为 mol·L-1·min-1。
2NH3 △H<0。若保持温度不变,某兴趣小组同学测得反应过程中容器内压强随时间变化如图所示:8 min内分钟NH3的平均生成速率为 mol·L-1·min-1。
(2)仍在T℃时,将0.6molH2和0.4molN2置于一容积可变的密闭容 器中。
①下列各项能说明该反应已达到平衡状态的是 (填序号)。
a.容器内N2、H2、NH3的浓度之比为l:3:2
b.3v正(N2)=v逆(H2)
c.3v正(H2)=2v逆(NH3)
d.混合气体的密度保持不变
e.容器中气体的平均相对分子质量不随时间而变化
②该条件下达到平衡时NH3的体积分数与题(1)条件下NH3的体积分数相比 (填“变大”“变小”或“不变”)。
③达到平衡后,改变某一条件使反应速率发生了如图所示的变化,改 变的条件可能是 。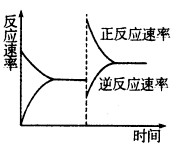
a.升高温度,同时加压
b.降低温度,同时减压
c.保持温度、压强不变,增大反应物浓度
d.保持温度、压强不变,减小生成物浓度
(3)硝酸厂的尾气含有氮氧化物,不经处理直接排放将污染空气。 氨气能将氮氧化物还原为氮气和水,其反应机理为:
2NH3(g)+5NO2(g)=7NO(g)+3H2O(g)  H=-akJ·mol-1
H=-akJ·mol-1
4NH3(g)+6NO(g)=5N2(g)+6H2O(g)  H=-bkJ·mol-1
H=-bkJ·mol-1
则NH3直接将NO2还原为N2的热化学方程式为: 。
若标准状况下NO与NO2混合气体40.32L被足量氨水完全吸收,产生标准状况下氮气42.56L。该混合气体中NO与NO2的体积之比为 。
(1)0.0125;(2)①bde;②变大;③c;
(3)8NH3(g)+6NO2(g)=7N2(g)+12H2O(g) △H=—(6a+7b)/5kJ·mol-1;1:2。
解析试题分析:(1)分析题给图像知,反应体系中的压强由起始状态的m变为平衡状态的0.8m,根据阿伏加德罗定律:在等温等容的条件下,气体的压强之比等于气体的物质的量之比知,容器内气体的总物质的量为反应前的1.0mol变为平衡后的0.8mol,气体的物质的量减少0.2mol;结合反应3H2+N2 2NH3利用差量法分析知,生成气体减少的物质的量与生产氨气的物质的量的相等,为0.2mol,根据公式v=△n/V△t计算得8 min内分钟NH3的平均生成速率为0.0125mol·L-1·min-1;(2)① a.平衡时N2、H2、NH3的浓度之比不一定为l:3:2,错误;b.由3v正(N2)=v逆(H2)得v正(N2):v逆(H2)=1:3,等于化学计量数之比,正确;c.由3v正(H2)=2v逆(NH3)得v正(H2):v逆(NH3)=2:3,不等于化学计量数之比,错误;d.由于反应在容积可变的密闭容器中进行,混合气体的密度随反应的进行不断变化,当其保持不变时已达平衡,正确;e.容器中气体的平均相对分子质量不随时间而变化,已达平衡,正确,选bde;②合成氨的反应正向为气体物质的量减小的反应,等温等压条件下达到平衡与等温等容条件下达到平衡相比,相当于缩小容器的体积,平衡正向移动,NH3的体积分数变大;③a.升高温度,同时加压,v正、v逆同时增大,与图像不符,错误;b.降低温度,同时减压,v正、v逆同时减小,与图像不符,错误;c.保持温度、压强不变,向容器内充入氮气或氢气来增大反应物浓度,v正增大,容器内气体物质的量增大,为保持压强不变,容器体积增大,氨气浓度减小,v逆减小,达平衡后速率可能比原平衡大,正确;d.保持温度、压强不变,从容器内分离出氨气来减小生成物浓度,v逆减小,容器内气体物质的量减小,为保持压强不变,容器体积减小,反应物浓度增大,v正增大,根据等效平衡知识知,达平衡后速率与原平衡相等,与图像不符,错误,选c;(3)根据反应①2NH3(g)+5NO2(g)=7NO(g)+3H2O(g) △H=-akJ·mol-1
2NH3利用差量法分析知,生成气体减少的物质的量与生产氨气的物质的量的相等,为0.2mol,根据公式v=△n/V△t计算得8 min内分钟NH3的平均生成速率为0.0125mol·L-1·min-1;(2)① a.平衡时N2、H2、NH3的浓度之比不一定为l:3:2,错误;b.由3v正(N2)=v逆(H2)得v正(N2):v逆(H2)=1:3,等于化学计量数之比,正确;c.由3v正(H2)=2v逆(NH3)得v正(H2):v逆(NH3)=2:3,不等于化学计量数之比,错误;d.由于反应在容积可变的密闭容器中进行,混合气体的密度随反应的进行不断变化,当其保持不变时已达平衡,正确;e.容器中气体的平均相对分子质量不随时间而变化,已达平衡,正确,选bde;②合成氨的反应正向为气体物质的量减小的反应,等温等压条件下达到平衡与等温等容条件下达到平衡相比,相当于缩小容器的体积,平衡正向移动,NH3的体积分数变大;③a.升高温度,同时加压,v正、v逆同时增大,与图像不符,错误;b.降低温度,同时减压,v正、v逆同时减小,与图像不符,错误;c.保持温度、压强不变,向容器内充入氮气或氢气来增大反应物浓度,v正增大,容器内气体物质的量增大,为保持压强不变,容器体积增大,氨气浓度减小,v逆减小,达平衡后速率可能比原平衡大,正确;d.保持温度、压强不变,从容器内分离出氨气来减小生成物浓度,v逆减小,容器内气体物质的量减小,为保持压强不变,容器体积减小,反应物浓度增大,v正增大,根据等效平衡知识知,达平衡后速率与原平衡相等,与图像不符,错误,选c;(3)根据反应①2NH3(g)+5NO2(g)=7NO(g)+3H2O(g) △H=-akJ·mol-1
②4NH3(g)+6NO(g)=5N2(g)+6H2O(g) △H=-bkJ·mol-1利用盖斯定律:(①×6+②×7)÷5得NH3直接将NO2还原为N2的热化学方程式为:③8NH3(g)+6NO2(g)=7N2(g)+12H2O(g) △H=—(6a+7b)/5kJ·mol-1;根据反应②和③列方程组计算;设NO的物质的量为x,NO2的物质的量为y,根据题意知,x+y=40.32/22.4mol=1.8mol,5/6x+7/6y=42.56/22.4mol=1.9mol解得x=0.6mol,y=1.2mol;则该混合气体中NO与NO2的体积之比为1:2。
考点:考查化学反应速率和化学平衡及相关图像、盖斯定律及根据化学方程式计算。

 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的量随时间变化的曲线如图所示: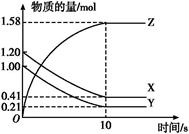
(1)从反应开始到10 s时,用Z表示的反应速率为 ,X的物质的量浓度减少了 ,Y的转化率为 。
(2)该反应的化学方程式为
(3)10 s后的某一时刻(t1)改变了外界条件,其速率随时间的变化图像如图所示: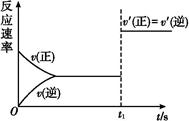
则下列说法符合该图像的是 。
| A.t1时刻,增大了X的浓度 | B.t1时刻,升高了体系温度 |
| C.t1时刻,缩小了容器体积 | D.t1时刻,使用了催化剂 |
据报道,在300 ℃、70 MPa 条件下,由CO2和H2合成乙醇已成为现实,该合成对解决能源问题具有重大意义。
(1)已知25 ℃、101 kPa条件下,1 g乙醇燃烧生成CO2和液态水时释放出a kJ能量,请写出该条件下乙醇燃烧的热化学反应方程式: 。
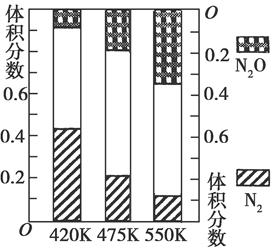
(2)由CO2和H2合成乙醇的化学方程式为2CO2(g)+6H2(g) CH3CH2OH(g)+3H2O(g)。实验测得温度对反应的影响如图所示。
CH3CH2OH(g)+3H2O(g)。实验测得温度对反应的影响如图所示。
①正反应的ΔH 0(填“>”、“<”或“=”);
②该反应的化学平衡常数表达式为K= 。
(3)对于该化学平衡,为了提高H2的转化率,可采取的措施有 。
| A.升温 | B.加压 |
| C.加催化剂 | D.增加CO2的浓度 |
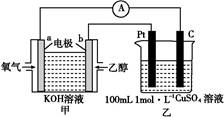
①b电极上发生的电极反应式为 。
②若甲中有0.1 mol CH3CH2OH参加反应,则乙装置中生成的气体在标准状况下的体积共为 L。
已知CO2(g)+H2(g) CO(g)+H2O(g)的平衡常数随温度变化如下表:
CO(g)+H2O(g)的平衡常数随温度变化如下表:
| t/℃ | 700 | 800 | 850 | 1 000 | 1 200 |
| K | 2.6 | 1.7 | 1.0 | 0.9 | 0.6 |
请回答下列问题:
(1)上述正向反应是________反应(选填“放热”或“吸热”)。
(2)能判断该反应达到化学平衡状态的依据是________。(填编号)
A.容器中压强不变
B.c(CO2)=c(CO)
C.生成a mol CO2的同时消耗a mol H2
D.混合气体的平均相对分子质量不变
E.混合气体的密度不变
(3)在850 ℃发生上述反应,以表中的物质的量投入恒容反应器中,其中向正反应方向进行的有________(选填A、B、C、D、E)。
| | A | B | C | D | E |
| n(CO2) | 3 | 1 | 0 | 1 | 1 |
| n(H2) | 2 | 1 | 0 | 1 | 2 |
| n(CO) | 1 | 2 | 3 | 0.5 | 3 |
| n(H2O) | 5 | 2 | 3 | 2 | 1 |
(4)在850 ℃时,可逆反应:CO2(g)+H2(g)
 CO(g)+H2O(g),在该容器内各物质的浓度变化如下:
CO(g)+H2O(g),在该容器内各物质的浓度变化如下:| 时间 /min | CO2 (mol·L-1) | H2 (mol·L-1) | CO (mol·L-1) | H2O (mol·L-1) |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
则3 min~4 min平衡后c3=________mol·L-1,CO2的转化率为________。
煤化工中常需研究不同温度下平衡常数、投料比及热值等问题。
已知:CO(g)+H2O(g)  H2(g)+CO2(g)平衡常数随温度的变化如下表:
H2(g)+CO2(g)平衡常数随温度的变化如下表:
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
(1)在800℃发生上述反应,以表中的物质的量投入恒容反应器,其中向正反应方向移动的有 (选填A、B、C、D、E);
| | n(CO) | n(H2O) | n(H2) | n(CO2) |
| A | 1 | 5 | 2 | 3 |
| B | 2 | 2 | 1 | 1 |
| C | 3 | 3 | 0 | 0 |
| D | 0.5 | 2 | 1 | 1 |
| E | 3 | 1 | 2 | 1 |
(3)已知在一定温度下,C(s)+CO2(g)
 2CO(g)平衡常数K;K的表达式 ;
2CO(g)平衡常数K;K的表达式 ;C(s)+H2O(g)
 CO(g)+H2(g) 平衡常数K1;
CO(g)+H2(g) 平衡常数K1;CO(g)+H2O(g)
 H2(g)+CO2(g)平衡常数K2;
H2(g)+CO2(g)平衡常数K2;则K、K1、K2之间的关系是: ;
(4)某温度下C(s)+CO2(g)
 2CO(g)能判断该反应达到化学平衡状态的依据是________。
2CO(g)能判断该反应达到化学平衡状态的依据是________。A.c(CO2)=c(CO) B.K不变 C.容器中的压强不变
D.v正(CO)=2v正(CO2) E.c(CO)保持不变 F.混合气体相对分子质量不变
(5)如图1所示,在甲、乙两容器中都充入1molC和1molCO2,并使甲、乙两容器初始容积相等。在相同温度下发生反应C(s)+CO2(g)
 2CO(g),并维持反应过程中温度不变。已知甲容器中
2CO(g),并维持反应过程中温度不变。已知甲容器中CO2的转化率随时间变化的图像如图2所示,请在图2中画出乙容器中CO2的转化率随时间变化的图像。
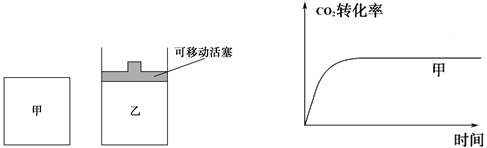
图1 图2
 cC(s)+dD,当反应进行到第t min时,测得A减少了n mol,B减少了n/2 mol,C增加了3n/2 mol,D增加了n mol。此时反应达到平衡。
cC(s)+dD,当反应进行到第t min时,测得A减少了n mol,B减少了n/2 mol,C增加了3n/2 mol,D增加了n mol。此时反应达到平衡。 2NH3(g) ΔH=-94.4 kJ·mol-1。恒容时,体系中各物质浓度随时间变化的曲线如图所示。
2NH3(g) ΔH=-94.4 kJ·mol-1。恒容时,体系中各物质浓度随时间变化的曲线如图所示。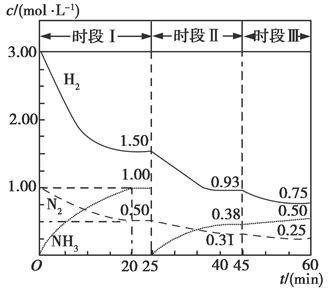

 Fe(s)+CO2(g)ΔH>0,已知1 373 K时K=0.263。
Fe(s)+CO2(g)ΔH>0,已知1 373 K时K=0.263。