题目内容
【题目】实验室常用Na2O2与H2O反应快速制取少量O2.用下面装置制取O2并演示Na在O2中的燃烧实验.
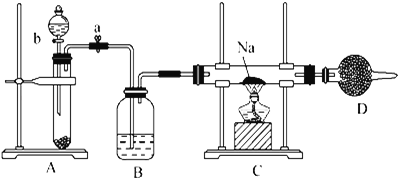
请回答下列问题:
(1)写出A装置中反应的化学方程式_____.
(2)B装置中盛放的试剂是_____.
(3)D装置中盛放的试剂是_____,其作用是_____.
【答案】2Na2O2+2H2O =4NaOH+O2↑ 浓硫酸 碱石灰 防止空气中的H2O、CO2进入C装置
【解析】
由图,A装置中过氧化钠和水反应制得的氧气会进入C装置中和Na单质发生燃烧反应,在制取O2的过程中会带有水蒸气,若水蒸气进入C装置中会和Na单质反应,所以在A装置和C装置之间放入一个干燥装置B吸收水蒸气,同理D装置放于尾部是为了防止空气中的水蒸气和CO2进入C装置中与Na单质、Na2O2反应。
(1)A装置中过氧化钠和水反应制得氧气,化学方程式:2Na2O2+2H2O =4NaOH+O2↑;
(2)A装置和C装置之间放入一个干燥装置吸收水蒸气,B装置中盛放的试剂是:浓硫酸;
(3)D装置放于尾部是为了防止空气中的水蒸气和CO2进入C装置中与Na单质、Na2O2反应,影响实验现象的判断,干燥管中应装碱石灰。

练习册系列答案
相关题目