题目内容
11.三草酸合铁(Ⅲ)酸钾晶体K3[Fe(C2O4)3]•3H2O可用于摄影和蓝色印刷.可用如下流程来制备.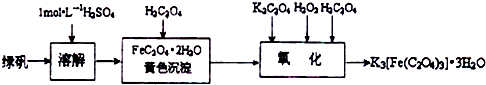
根据题意完成下列各题:
(1)若用铁和稀硫酸制备FeSO4•7H2O,铁(填物质名称)往往要过量.
(2)要从溶液中得到绿矾,必须进行的实验操作是bcae.(按前后顺序填)
a.过滤洗涤 b.蒸发浓缩 c.冷却结晶 d.灼烧 e.干燥
某课外化学兴趣小组为测定三草酸合铁酸钾晶体(K3[Fe(C2O4)3]•3H2O)中铁元素含量,做了如下实验:
步骤一:称量5.000g三草酸合铁酸钾晶体,配制成250ml溶液.
步骤二:取所配溶液25.00ml于锥形瓶中,加稀H2SO4酸化,滴加KMnO4溶液至草酸根恰好全部被氧化成
二氧化碳,同时,MnO${\;}_{4}^{-}$.被还原成Mn2+.向反应后的溶液中加入一定量锌粉,加热至黄色刚好消失,过
滤,洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时,溶液仍里酸性.
步骤三:用0.010mol/L KMnO4溶液滴定步骤二所得溶液至终点,消耗KMnO4溶液20.02ml,滴定中MnO4-,
被还原成Mn2+.
重复步骤二、步骤三操作,滴定消耗0.010mol/LKMnO4溶液19.98ml;
(3)配制三草酸合铁酸钾溶液需要使用的玻璃仪器除烧杯、玻璃棒以外还有250ml容量瓶;主要操作步骤依次是:称量、溶解、转移、洗涤、定容、摇匀.
(4)加入锌粉的目的是将Fe3+还原成Fe2+,为进一步测定铁元素的含量做准备.
(5)实验测得该晶体中铁的质量分数为11.12%.在步骤二中,若加入的KMnO4的溶液的量不够,则测得的铁含量偏高.(选填“偏低”“偏高”“不变”)
(6)某同学将8.74g无水三草酸合铁酸钾(K3[Fe(C2O4)3])在一定条件下加热分解,所得固体的质量为5.42g,同时得到密度为1.647g/L(已折合成标准状况下)气体.研究固体产物得知,铁元素不可能以三价形式存在,而盐只有K2CO3.写出该分解反应的化学方程式2K3[Fe(C2O4)3]═3K2CO3+Fe+FeO+4CO↑+5CO2↑.
分析 (1)亚铁离子易被空气中的氧气氧化为铁离子,需要加入过量的铁粉避免亚铁离子被氧化;
(2)根据溶液来得到晶体来分析实验操作;
(3)根据实验操作的步骤以及每步操作需要仪器确定反应所需仪器;
(4)锌粉能与Fe3+反应,加入锌粉的目的是将Fe3+恰好还原成Fe2+;
(5)依据化学方程式或离子方程式计算,注意配制溶液的体积变化;加入的KMnO4的溶液的量不足,导致草酸根有剩余,再滴定亚铁离子时,进行与高锰酸钾反应,使的滴定亚铁离子消耗的高锰酸钾的体积偏大;
(6)根据气体的密度为求出其摩尔质量,然后根据摩尔质量和质量守恒来判断成分;依据信息:固体产物中,铁元素不可能以三价形式存在,而盐只有K2CO3,结合电子得失守恒,可推测铁元素只能以亚铁和铁单质的形式存在;最后写出方程式.
解答 解:(1)亚铁离子易被空气中的氧气氧化为铁离子,需要加入过量的铁粉避免亚铁离子被氧化,2Fe3++Fe=3Fe2+;
故答案为:铁;
(2)将混合液来制备绿矾时应先将溶液加热浓缩、然后冷却结晶,将析出的固体过滤、洗涤、干燥,即可得到绿矾,
故答案为:bcae;
(3)配制步骤有计算、称量、溶解、冷却、移液、洗涤、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解,冷却后转移到250mL容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,所以需要的仪器为:托盘天平、药匙、烧杯、玻璃棒、250mL容量瓶、胶头滴管;
故答案为:250ml容量瓶;溶解,洗涤;
(4)向反应后的溶液中加入一小匙锌粉,加热至溶液完全由黄色变为浅绿色,说明加入锌粉的目的是将Fe3+恰好还原成Fe2+;
故答案为:将Fe3+还原成Fe2+,为进一步测定铁元素的含量做准备;
(5)再重复(1)、(2)步骤两次,滴定消耗0.01moL/KMnO4溶液平均体积为19.98mL;
5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O
5mol 1mol
n(Fe2+) 0.010×0.01998mol
配制成250moL溶液,取所配溶液25.00moL进行的中和滴定实验,含亚铁离子物质的量n(Fe2+)=5×0.010×0.01998mol:所以250ml溶液中亚铁离子物质的量为:10×5×0.010×0.01998mol:铁的质量分数ω(Fe)=[10×5×0.010×0.01998mol×56 g/mol]÷5.000 g×100%=11.12%;
加入的KMnO4的溶液的量不足,导致草酸根有剩余,再滴定亚铁离子时,进行与高锰酸钾反应,使的滴定亚铁离子消耗的高锰酸钾的体积偏大,导致测定的亚铁离子的物质的量偏大,故铁元素的质量偏大,计算测定的铁元素的质量分数偏高,
故答案为:11.12%;偏高;
(6)气体密度为1.647g/L,其摩尔质量为1.647g/L×22.4L/mol=36.9g/mol,所以气体为CO和C02,两者的物质的量之比$\frac{44-36.9}{36.9-28}$=$\frac{4}{5}$,固体产物中,铁元素不可能以三价形式存在,而盐只有K2CO3,结合电子得失守恒,可推测铁元素只能以亚铁和铁单质的形式存在,故方程式为:2K3[Fe(C2O4)3]═3K2CO3+Fe+FeO+4CO↑+5CO2↑;
故答案为:2K3[Fe(C2O4)3]═3K2CO3+Fe+FeO+4CO↑+5CO2↑.
点评 本题考查较为综合,涉及到溶液的配制、滴定操作的指示剂选择,氧化还原反应的离子方程式的书写,化学方程式的计算,注意基础实验知识的积累,把握实验步骤、原理和注意事项等问题.

| A. | 钠与水反应:Na+H2O═Na++OH-+H2↑ | |
| B. | 向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液使SO42-反应完全:2Ba2++4OH-+Al3++2SO42-═2BaSO4↓+AlO2-+2H2O | |
| C. | 硫酸铜溶液与氢氧化钡溶液反应:Ba2++SO42-═BaSO4↓ | |
| D. | 向Fe(NO3)2溶液中加入稀盐酸:3Fe2++4H++NO3-═3Fe3++NO↑+2H2O |
| A. | 用物质A表示的反应的平均速率为0.3 mol•L-1•s-1 | |
| B. | 2s时的压强是起始时的1.1倍 | |
| C. | 2s时物质A的转化率为30% | |
| D. | 2s时物质B的浓度为0.7mol/L |
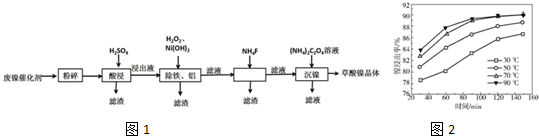
已知:①Ksp(CaF2)=1.46×10-10,Ksp(CaC2O4)=2.34×10-9.
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Al3+ | 3.0 | 5.0 |
| Ni2+ | 6.7 | 9.5 |
(1)“粉碎”的目的是增大接触面积,加快反应速率,提高镍的浸出率.
(2)保持其他条件相同,在不同温度下对废镍催化剂进行“酸浸”,镍浸出率随时间变化如图2.“酸浸”的适宜温度与时间分别为c(填字母).
a.30℃、30min b.90℃、150min c.70℃、120min d.90℃、120min
(3)证明“沉镍”工序中Ni2+已经沉淀完全的实验步骤及现象 是静置,在上层清液中继续滴加(NH4)2C2O4溶液,若不产生沉淀,则Ni2+已经沉淀完全.将“沉镍”工序得到的混合物过滤,所得固体用75%乙醇溶液洗涤、110℃下烘干,得草酸镍晶体.用75%乙醇溶液洗涤的目的是洗去(NH4)2SO4杂质、便于烘干、减少草酸镍晶体损失.
(4)在除铁和铝工序中,应先加入H2O2氧化,再加氢氧化镍调节pH值的范围为5.0≤pH<6.7.第2步中加入适量NH4F溶液的作用是除去杂质Ca2+.
(5)将得到的草酸镍晶体在真空中加热至320℃分解可重新制得单质镍催化剂,写出该制备过程的化学方程式:NiC2O4•2H2O$\frac{\underline{\;320℃\;}}{\;}$Ni+2CO2↑+2H2O.
(6)已知废镍催化剂中镍的质量分数为5.9%,则100kg废镍催化剂最多可制得18.3kg草酸镍晶体(Ni:59,C:12,H:1,O:16).
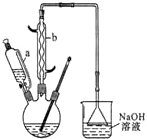 己二酸是合成尼龙-66的主要原料之一.实验室合成己二酸的原理、有关数据及装置示意图如图表:
己二酸是合成尼龙-66的主要原料之一.实验室合成己二酸的原理、有关数据及装置示意图如图表: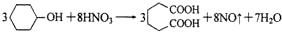
| 物质 | 密度(g/cm3) | 熔点 | 沸点 | 溶解性 |
| 环己醇 | 0.962g/cm3 | 25.9℃ | 160.8℃ | 20℃时水中溶解度为3.6g,可混溶于乙醇、苯 |
| 己二酸 | 1.360g/cm3 | 152℃ | 337.5℃ | 在水中的溶解度:15℃时1.44g,25℃时2.3g,易溶于乙醇、不溶于苯 |
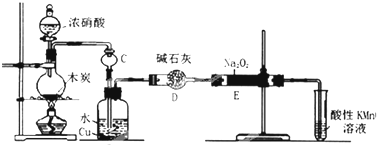
Ⅰ.在三口烧瓶中加入16mL 50%的硝酸(密度为l.3lg/cm3),再加入1~2粒沸石,滴液漏斗中盛放有5.4mL环己醇.
Ⅱ.水浴加热三口烧瓶至50℃左右,移去水浴,缓慢滴加5~6滴环己醇,摇动三口烧瓶,观察到有红棕色气体放出时再慢慢滴加剩下的环己醇,维持反应温度在60℃~65℃之间.
Ⅲ.当环己醇全部加入后,将混合物用80℃一90℃水浴加热约10min(注意控制温度),直至无红棕色气体生成为止.
Ⅳ.趁热将反应液倒入烧杯中,放入冰水浴中冷却,析出晶体后过滤、洗涤、干燥、称重.
请回答下列问题:
(1)本实验所用50%的硝酸物质的量浓度为10.4 mol/L.滴液漏斗的细支管a的作用是平衡滴液漏斗与三口烧瓶内的气压,使环己醇能够顺利流下.
(2)仪器b的名称为球形冷凝管(或冷凝管).,使用时要从下口(填“上口”或“下口”)通入冷水.
(3)NaOH溶液的作用是吸收NO2,防止污染空气,溶液上方倒扣的漏斗作用是防止液体倒吸.
(4)向三口烧瓶中滴加环己醇时,反应温度迅速上升,为使反应温度不致过高,必要时可采取的措施是将三口烧瓶置于冷水浴中.
(5)进行该实验时要控制好环己醇的滴入速率,防止反应过于剧烈,否则可能造成较严重的后果,试列举两条可能的后果:反应液暴沸冲出冷凝管;放热过多可能引起爆炸;产生的二氧化氮气体来不及被碱液吸收而外逸到空气中.
(6)为了除去可能的杂质和减少产品损失,可分别用冰水和苯洗涤晶体.
| A. | CO+H2O?CO2+H2 | B. | H2PO4-+H2O?HPO42-+H3O+ | ||
| C. | Cl-+H2O?HCl+OH- | D. | HS-+H2O?H2S+OH- |