题目内容
1.下列方程式中,属于水解反应的是( )| A. | CO+H2O?CO2+H2 | B. | H2PO4-+H2O?HPO42-+H3O+ | ||
| C. | Cl-+H2O?HCl+OH- | D. | HS-+H2O?H2S+OH- |
分析 水解反应是盐中的弱离子和水电离出来的氢离子或是氢氧根离子结合生成弱电解质的反应,据此回答.
解答 解:A、反应不是弱离子参与的反应,不属于水解反应,故A错误;
B、该式子是弱酸根阴离子的电离方程式,不是水解反应,故B错误;
C、氯离子是强酸的阴离子,不能发生水解反应,故C错误;
D、硫氢根离子是弱酸的阴离子,可以和水电离出的氢离子之间反应,属于水解反应,故D正确.
故选D.
点评 本题考查学生盐的水解原理以及方程式的书写知识,属于基本知识的考查,难度中等.

练习册系列答案
 寒假学与练系列答案
寒假学与练系列答案
相关题目
9.现有①液态氧 ②氢氧化铁胶体 ③食盐水 ④纯碱 ⑤氢氧化钾 ⑥空气 对上述物质的分类全部正确的是( )
| A. | 盐 ③④ | B. | 混合物 ②③⑥ | C. | 纯净物 ④⑤⑥ | D. | 碱 ④⑤ |
6.25℃时,水中存在电离平衡:H2O═H++OH-△H>0.下列叙述正确的是( )
| A. | 将水加热,Kw增大,pH不变 | |
| B. | 向水中加入少量NaHSO4固体,溶液的c(H+)增大,水电离的c(H+)降低 | |
| C. | 向水中加入少量NaOH固体,平衡逆向移动,溶液的c(OH-)降低 | |
| D. | 向水中加入少量NH4Cl固体,平衡正向移动,溶液的c(OH-)增大 |
13.下列说法正确的是( )
| A. | △H>0,△S>0 的反应任何条件都是非自发反应 | |
| B. | 放热反应均能自发进行,且反应放出的热量越多,反应越完全 | |
| C. | 某反应的△H>0、△S<0,则该反应一定不能正向进行 | |
| D. | 水从固态→液态→气态的变化过程中△S>0 |
10.下列说法正确的是( )
| A. | 根据酸分子中含有的H原子个数将酸分为一元酸、二元酸、多元酸 | |
| B. | 酸性氧化物都是非金属氧化物 | |
| C. | Na2O熔融状态下能导电,所以Na2O是电解质 | |
| D. | 胶体区别于其他分散系的本质特征是产生丁达尔效应 |
11.乙烯和苯能够共同发生的反应类型有( )
①加成反应
②取代反应
③聚合反应
④氧化反应.
①加成反应
②取代反应
③聚合反应
④氧化反应.
| A. | ①② | B. | ②③ | C. | ③④ | D. | ①④ |
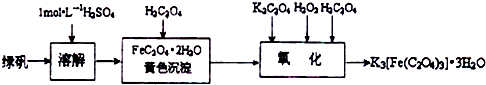
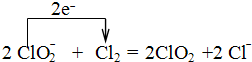 .
.