题目内容
19.草酸镍晶体(NiC2O4•2H2O)可用于制镍催化剂,某小组用废镍催化剂(成分为Al2O3、Ni、Fe、SiO2、CaO等)制备草酸镍晶体的部分实验流程如下如图1: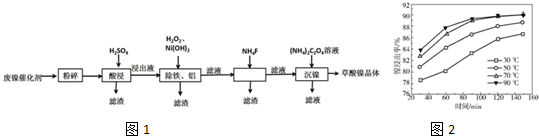
已知:①Ksp(CaF2)=1.46×10-10,Ksp(CaC2O4)=2.34×10-9.
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Al3+ | 3.0 | 5.0 |
| Ni2+ | 6.7 | 9.5 |
(1)“粉碎”的目的是增大接触面积,加快反应速率,提高镍的浸出率.
(2)保持其他条件相同,在不同温度下对废镍催化剂进行“酸浸”,镍浸出率随时间变化如图2.“酸浸”的适宜温度与时间分别为c(填字母).
a.30℃、30min b.90℃、150min c.70℃、120min d.90℃、120min
(3)证明“沉镍”工序中Ni2+已经沉淀完全的实验步骤及现象 是静置,在上层清液中继续滴加(NH4)2C2O4溶液,若不产生沉淀,则Ni2+已经沉淀完全.将“沉镍”工序得到的混合物过滤,所得固体用75%乙醇溶液洗涤、110℃下烘干,得草酸镍晶体.用75%乙醇溶液洗涤的目的是洗去(NH4)2SO4杂质、便于烘干、减少草酸镍晶体损失.
(4)在除铁和铝工序中,应先加入H2O2氧化,再加氢氧化镍调节pH值的范围为5.0≤pH<6.7.第2步中加入适量NH4F溶液的作用是除去杂质Ca2+.
(5)将得到的草酸镍晶体在真空中加热至320℃分解可重新制得单质镍催化剂,写出该制备过程的化学方程式:NiC2O4•2H2O$\frac{\underline{\;320℃\;}}{\;}$Ni+2CO2↑+2H2O.
(6)已知废镍催化剂中镍的质量分数为5.9%,则100kg废镍催化剂最多可制得18.3kg草酸镍晶体(Ni:59,C:12,H:1,O:16).
分析 废镍催化剂(成分为Al2O3、Ni、Fe、SiO2、CaO等),用硫酸溶解,SiO2不与硫酸反应,过滤得到滤液中含有NiSO4、FeSO4、Al2(SO4)3、CaSO4及过量的硫酸,加入H2O2将Fe2+氧化为Fe3+,加入Ni(HO)2调节pH,使pH大于5.0小于6.8,Fe3+转化为Fe(OH)3沉淀、Al3+转化为Al(OH)3沉淀,过滤除去,滤液中含有NiSO4、CaSO4,向滤液中加入NH4F,除去Ca 2+,过滤,再向滤液中加入(NH4)2C2O4,得到草酸镍沉淀,再过滤、洗涤、干燥得草酸镍晶体,
(1)把废镍催化剂粉碎,增大了反应的接触面积,加快反应速率,提高镍的浸出率;
(2)根据镍浸出率随时间变化图可知,70℃时,镍浸出率很大,从时间看,120min镍浸出率就已经很高了;
(3)“沉镍”工序中,可以用继续滴加(NH4)2C2O4溶液的方法,检验Ni2+是否沉淀完全,待溶液静置后,在上层清液中继续滴加(NH4)2C2O4溶液,若不产生沉淀,则Ni2+已经沉淀完全;“沉镍”工序生成了(NH4)2SO4,用乙醇洗涤,能洗去(NH4)2SO4杂质、便于烘干;
(4)为了除去铁、铝元素,取“浸出液”,用双氧水氧化二价铁为三价铁,再加入NaOH溶液,调节溶液5.0≤pH≤6.7,让Al3+、Fe3+沉淀完全,不能让Ni2+沉淀;根据Ksp(CaF2)=1.46×10-10<Ksp(CaC2O4)=2.34×10-9,加入适量NH4F溶液,生成CaF2,除去Ca2+;
(5)草酸镍晶体(NiC2O4•2H2O)在320℃分解得到Ni、CO2和H2O;
(6)根据关系式:Ni~NiC2O4•2H2O计算.
解答 解:废镍催化剂(成分为Al2O3、Ni、Fe、SiO2、CaO等),用硫酸溶解,SiO2不与硫酸反应,过滤得到滤液中含有NiSO4、FeSO4、Al2(SO4)3、CaSO4及过量的硫酸,加入H2O2将Fe2+氧化为Fe3+,加入Ni(HO)2调节pH,使pH大于5.0小于6.8,Fe3+转化为Fe(OH)3沉淀、Al3+转化为Al(OH)3沉淀,过滤除去,滤液中含有NiSO4、CaSO4,向滤液中加入NH4F,除去Ca 2+,过滤,再向滤液中加入(NH4)2C2O4,得到草酸镍沉淀,再过滤、洗涤、干燥得草酸镍晶体,
(1)把废镍催化剂粉碎,增大了反应的接触面积,加快反应速率,提高镍的浸出率,
故答案为:增大接触面积,加快反应速率,提高镍的浸出率;
(2)根据镍浸出率随时间变化图可知,70℃时,镍浸出率很大,从时间看,120min镍浸出率就已经很高了,
故答案为:c;
(3)“沉镍”工序中,可以用继续滴加(NH4)2C2O4溶液的方法,检验Ni2+是否沉淀完全,待溶液静置后,在上层清液中继续滴加(NH4)2C2O4溶液,若不产生沉淀,则Ni2+已经沉淀完全;“沉镍”工序生成了(NH4)2SO4,用乙醇洗涤,能洗去(NH4)2SO4杂质、便于烘干、减少草酸镍晶体损失,
故答案为:静置,在上层清液中继续滴加(NH4)2C2O4溶液,若不产生沉淀,则Ni2+已经沉淀完全;洗去(NH4)2SO4杂质、便于烘干、减少草酸镍晶体损失;
(4)为了除去铁、铝元素,用双氧水氧化二价铁为三价铁,再加入NaOH溶液,调节溶液5.0≤pH≤6.7,让Al3+、Fe3+沉淀完全,不能让Ni2+沉淀;根据Ksp(CaF2)=1.46×10-10<Ksp(CaC2O4)=2.34×10-9,加入适量NH4F溶液,生成CaF2,除去Ca2+,
故答案为:5.0≤pH<6.7;除去杂质Ca2+;
(5)草酸镍晶体(NiC2O4•2H2O)在320℃分解得到Ni、CO2和H2O,反应的方程式为NiC2O4•2H2O$\frac{\underline{\;320℃\;}}{\;}$Ni+2CO2↑+2H2O;
故答案为:NiC2O4•2H2O$\frac{\underline{\;320℃\;}}{\;}$Ni+2CO2↑+2H2O;
(6)根据关系式:Ni~NiC2O4•2H2O
59 183
100kg×5.9% m,
解得m=18.3kg;
故答案为:18.3.
点评 本题考查了物质分离的实验设计和方法应用,主要是利用溶液不同pH条件下离子沉淀的情况不同,控制溶液PH除去杂质离子,得到较纯净的硫酸镍溶液来制备硫酸镍晶体,同时考查了除杂原则不能引入新的杂质,题目难度大.

 学业测评一课一测系列答案
学业测评一课一测系列答案 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案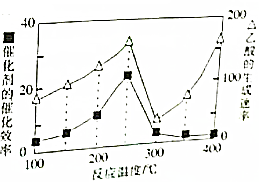 用甲烷和二氧化碳可以制备化工原料.
用甲烷和二氧化碳可以制备化工原料.(1)一定温度下,向容积恒定为2L的密闭容器中通入3mol CO2、3mol CH4,发生如下反应:CO2(g)+CH4(g)?2CO(g)+2H2(g),反应在2min末达到平衡状态,此时测得CO2和CO的体积分数相等,请回答下列问题:
①2min内,用H2来表示的反应速率v(H2)=0.5mol/L•min;
②此时温度下该反应的平衡常数K=1;
③下列叙述可以作为该反应达到平衡状态的标志的是BC(填选项字母)
A.v正(CH4)=2v逆(H2)
B.容器内压强保持恒定不变
C.反应中断裂2molC-H键同时消耗1mol H2
D.容器内混合气体的密度保持恒定不变
④已知:
| 物质 | H2 | CO | CH4 | CH3COOH |
| 燃烧热(KJ/mol) | 286 | 283 | 890 | 874 |
⑤为提高CH4的转化率,可以采取的措施是减小反应压强、增大CO2的浓度(写两点).
(2)在催化作用下,甲烷和二氧化碳还可以直接转化成乙酸.
①在不同温度下乙酸的生成速率如图苏搜:在250-400℃范围内,乙酸的生成速率随温度变化的原因是温度超过250℃时,催化剂的催化效率降低.
②在250℃与400℃时乙酸的生成速率相近,请分析判断实际生产选择的最佳温度是250℃时,催化剂的催化效果最好,提高温度耗费较高的能量,并且低温条件有利于平衡向着正反应方向移动.
| A. | 向橙色的K2Cr2O7溶液中加适量的浓硫酸充分振荡后橙色变深 | |
| B. | 向装有少量Na2S2O3溶液的试管中滴加适量稀硫酸充分振荡后无明显变化 | |
| C. | 向装有淀粉和KI溶液的试管中滴加适量H2SO4充分振荡后溶液变蓝 | |
| D. | 向装有少量H2O2溶液的试管中加适量CuSO4溶液充分振荡后产生大量气泡 |
| A. | 1L溶液中含有0.2NA个NO3- | |
| B. | 1L溶液中所含的阴、阳离子总数为0.6NA个 | |
| C. | 0.5L溶液中Ba2+浓度是0.1mol/L | |
| D. | 500mL溶液中,含有NO3-的物质的量为0.2mol |
| A. | 盐 ③④ | B. | 混合物 ②③⑥ | C. | 纯净物 ④⑤⑥ | D. | 碱 ④⑤ |