题目内容
【题目】甲醇是重要的有机化工原料,目前世界甲醇年产量超过2.1×107吨,在能源紧张的今天,甲醇的需求也在增大。甲醇的合成方法是:
(ⅰ)CO(g)+2H2(g)=CH3OH(g) ΔH=-90.1kJ·mol-1
另外:(ⅱ)2CO(g)+O2(g)=2CO2(g) ΔH=-566.0kJ·mol-1
(ⅲ)2H2(g)+O2(g)=2H2O(l) ΔH=-572.0kJ·mol-1
回答下列问题:
(1)甲醇的燃烧热为__kJ·mol-1。
(2)在碱性条件下利用一氯甲烷(CH3Cl)水解也可制备少量的甲醇,该反应的化学方程式为__。
(3)若反应在密闭恒容绝热容器中进行,反应(iv)CO2(g)+H2(g)=CO(g)+H2O(g) ΔH=+41.1kJ·mol-1对合成甲醇反应中CO的转化率的影响是(_________)
a.增大 b.减小 c.无影响 d.无法判断
(4)在恒温恒容的密闭容器中发生反应(ⅰ),各物质的浓度如下表:
浓度/mol·L-1 时间/min | c(CO) | c(H2) | c(CH3OH) |
0 | 0.8 | 1.6 | 0 |
2 | 0.6 | x | 0.2 |
4 | 0.3 | 0.6 | 0.5 |
6 | 0.3 | 0.6 | 0.5 |
①x=__。
②前2min内H2的平均反应速率为v(H2)=__。该温度下,反应(ⅰ)的平衡常数K=__。(保留1位小数)
③反应进行到第2min时,改变了反应条件,改变的这个条件可能是(_________)
a.使用催化剂 b.降低温度 c.增加H2的浓度
(5)如图是温度、压强与反应(ⅰ)中CO转化率的关系:
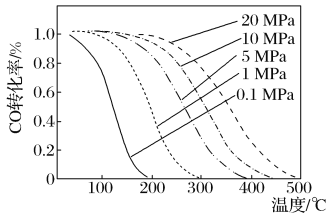
由图像可知,温度越低,压强越大,CO转化率越高,但实际生产往往采用300~400℃和10MPa的条件,其原因是__。
【答案】764.9 CH3Cl+NaOH→CH3OH+NaCl d 1.2 0.2mol·L-1·min-1 4.6L2·mol-2 a 温度较低,反应速率慢;压强太大,成本高
【解析】
(1)利用盖斯定律,热化学方程式(iii)-(i)+![]() (ii),得新的热化学方程式为:CH4OH(g)+
(ii),得新的热化学方程式为:CH4OH(g)+![]() O2(g)=CO2(g)+2H2O(l)△H=-764.9kJ·mol-1,故甲醇的燃烧热为764.9 kJ·mol-1;
O2(g)=CO2(g)+2H2O(l)△H=-764.9kJ·mol-1,故甲醇的燃烧热为764.9 kJ·mol-1;
(2)根据提示知CH3Cl中的Cl被羟基取代生成CH3OH,反应方程式为:CH3Cl+NaOH→CH3OH+NaCl[或CH3Cl+H2O![]() CH3OH+HCl];
CH3OH+HCl];
(3)反应(iv)消耗反应(i)的另外一种反应物氢气,而且生成反应(i)的反应物CO,使反应(i)的CO转化率降低;但反应(iv)为吸热反应,使体系温度降低,反应(i)正向移动,使反应(i)中CO的转化率提高,两个原因孰轻孰重不得而知,故无法判断反应(iv)对反应(i)中CO转化率的影响;
(4)①观察表中数据可知,0~2min内,CO浓度降低了0.2mol/L,则H2浓度会降低0.4mol/L,则x=1.6-0.4=1.2;
②![]() ;平衡常数
;平衡常数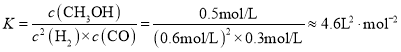 ;
;
③2min到4min的反应速率大于0到2min,而降低温度,反应速率降低,b项错误;由表格中的数据可知c项错误;故a项使用催化剂正确,故答案为:a;
(5)温度较低,反应速率慢,不利于甲醇的生成;压强越大,CO的转化率越大,但压强太大对设备要求高,成本高。

【题目】现使用酸碱中和滴定法测定市售白醋的总酸量(g·100 mL-1)。
Ⅰ.实验步骤
(1)配制待测白醋溶液,用____(填仪器名称)量取10.00 mL食用白醋,在____(填仪器名称)中用水稀释后转移到100 mL____(填仪器名称)中定容,摇匀即得待测白醋溶液。
(2)量取待测白醋溶液20.00 mL于锥形瓶中,向其中滴加2滴____作指示剂。
(3)读取盛装0.1000 mol/L NaOH溶液的碱式滴定管的初始读数。
(4)滴定。判断滴定终点的现象是____,达到滴定终点,停止滴定,并记录NaOH溶液的最终读数,重复滴定3~4次。
(5)如图是某次滴定时的滴定管中的液面,其读数为____mL。
![]()
Ⅱ.实验记录
滴定次数 实验数据(mL) | 1 | 2 | 3 | 4 |
V(样品) | 20.00 | 20.00 | 20.00 | 20.00 |
V(NaOH)(消耗) | 15.95 | 15.00 | 15.05 | 14.95 |
Ⅲ.数据处理与讨论
(6)按正确数据处理,得出c(市售白醋)=____mol/L,市售白醋总酸量=____g·100 mL-1。