题目内容
19.化学与生活、社会密切相关.下列说法不正确的是( )| A. | 氢氧化铝和碳酸氢钠都可以作为治疗胃酸过多的药剂 | |
| B. | 血液透析是利用了胶体的性质 | |
| C. | 在食品袋中放入盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化变质 | |
| D. | 碘是人体必需微量元素,所以要多吃富含碘单质的食物 |
分析 A.氢氧化铝和碳酸氢钠碱性较弱,可与胃酸反应;
B.人体血液属于胶体,不能透过半透膜;
C.硅胶具有开放的多孔结构,吸附性强,铁粉具有强还原性;
D.碘是人体必需微量元素,所以要多吃富含碘元素的食物.
解答 解:A.氢氧化铝和碳酸氢钠碱性较弱,可与胃酸反应,所以氢氧化铝和碳酸氢钠都可以作为治疗胃酸过多的药剂,故A正确;
B.透析是通过小分子经过半透膜扩散到水(或缓冲液)的原理,将小分子与生物大分子分开的一种分离技术,人体的血液属于胶体,不能透过半透膜,故B正确;
C.硅胶具有开放的多孔结构,吸附性强,可做食品的吸水剂,铁粉具有强还原性,可作抗氧化剂,故C正确;
D.碘是人体必需微量元素,所以要多吃富含碘元素的食物,故D错误.
故选D.
点评 本题考查了盐类的水解、胶体、硅胶、铁粉等物质的性质,题目难度不大,掌握物质的性质是解题的关键.

练习册系列答案
相关题目
7.下列离子方程式正确的是( )
| A. | 向稀HNO3中滴加Na2SO3溶液:SO32-+2H+=SO2↑+H2O | |
| B. | CuSO4溶液与过量浓氨水反应的离子方程式:Cu2++2NH3-H2O=Cu(OH)2↓+2NH4+ | |
| C. | 0.01mol/LNH4Al(SO4)2溶液与0.02mol/LBa(OH)2溶液等体积混合:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2 H2O | |
| D. | 向CuSO4溶液中加入Na2O2:2 Na2O2+2Cu2++2H2O=4Na++2Cu(OH)2↓+O2↑ |
8.下列离子反应方程式正确的是( )
| A. | 向溶Ca(ClO)2液中通入少量SO2:Ca2++3ClO-+SO2 +H2O═CaSO4 ↓+Cl-+2HClO | |
| B. | 1mol/L的NaAlO2 溶液和2.5mol/L的盐酸等体积均匀混合:2AlO2-+5H+═A l(OH)3 ↓+Al3++H2O | |
| C. | 将11.2L标准状况下的氯气通入200mL 2mol/LFeBr2 的溶液中,离子反应方程式为:2Fe2++8Br-+5Cl2 ═2Fe3++4Br2 +10Cl- | |
| D. | 氢氧化亚铁溶于稀硝酸中:Fe(OH)2 +2H+═Fe2++H2O |
2.将1molCO和1molNO2充入密闭容器中,在催化剂存在下发生反应NO2(g)+CO(g)?CO2(g)+NO(g)并达到化学平衡,发现有50%的CO转化为CO2.在其它条件不变的情况下,若将1molCO和2molNO2充入上述反应器中,则反应达到化学平衡时,混合气体中的CO2的体积分数是( )
| A. | $\frac{1}{9}$ | B. | $\frac{1}{6}$ | C. | $\frac{2}{9}$ | D. | $\frac{1}{3}$ |

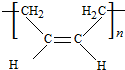
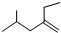 的系统命名4-甲基-2-乙基-1-戊烯.
的系统命名4-甲基-2-乙基-1-戊烯.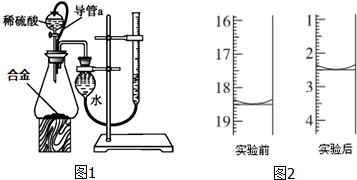 可利用以下方法测定铝镁合金(不含其它元素)组分含量
可利用以下方法测定铝镁合金(不含其它元素)组分含量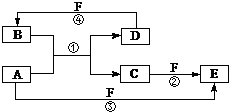 A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出).
A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出). ;反应④的化学方程式为:C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2+4NO2↑+2H2O.
;反应④的化学方程式为:C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2+4NO2↑+2H2O. ,反应①的化学方程式为2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑.
,反应①的化学方程式为2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑.