题目内容
10.将100g的碳酸钙放入氯化氢1.5mol的稀盐酸中,完全反应后可以生成二氧化碳0.75mol.分析 发生反应:CaCO3+2HCl═CaCl2+H2O+CO2↑,根据n=$\frac{m}{M}$计算碳酸钙的物质的量,进行过量计算,根据不足量的物质计算生成二氧化碳的物质的量.
解答 解:100g 碳酸钙的物质的量为$\frac{100g}{100g/mol}$=1mol,由CaCO3+2HCl═CaCl2+H2O+CO2↑,可知1mol碳酸钙完全反应消耗HCl为1mol×2=2mol>1.5mol,故HCl不足,则生成二氧化碳为1.5mol×$\frac{1}{2}$=0.75mol,
故答案为:0.75.
点评 本题考查化学方程式有关计算,涉及过量计算,比较基础,有利于基础知识的巩固.

练习册系列答案
相关题目
5.在一定条件下,将钠与氧气反应的生成物1.5g溶于水,所得溶液恰好能被50g质量分数为2.92%的盐酸中和.则该生成物的成分是( )
| A. | Na2O | B. | Na2O2 | C. | Na2O和Na2O2 | D. | 不能确定 |
15.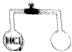 如图所示,已知两瓶容积相同,同温同压下,左瓶内充满氯化氢气体,当右瓶中充满下列混合气体中的某一组时,其所含原子总数与左瓶中所含原子总数一定相等,则该混合气体是( )
如图所示,已知两瓶容积相同,同温同压下,左瓶内充满氯化氢气体,当右瓶中充满下列混合气体中的某一组时,其所含原子总数与左瓶中所含原子总数一定相等,则该混合气体是( )
 如图所示,已知两瓶容积相同,同温同压下,左瓶内充满氯化氢气体,当右瓶中充满下列混合气体中的某一组时,其所含原子总数与左瓶中所含原子总数一定相等,则该混合气体是( )
如图所示,已知两瓶容积相同,同温同压下,左瓶内充满氯化氢气体,当右瓶中充满下列混合气体中的某一组时,其所含原子总数与左瓶中所含原子总数一定相等,则该混合气体是( )| A. | O3、N2 | B. | CH4、NH3 | C. | N2、O2 | D. | CO、CO2 |
5.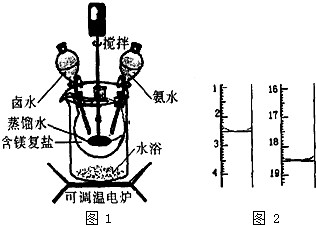 碱式碳酸镁密度小,是橡胶制品的优良填料.可用复盐MgCO3•(NH4)2CO3•H2O作原料制各.取一定量的含镁复盐放三颈烧瓶中,并将三颈烧瓶放在恒温水浴锅中加热(如图1所示),按一定的液固比加入蒸馏水,开启搅拌器同时加入预定的氨水,待温度到达40℃时开始热解,此时滴加卤水(氯化镁溶液)并继续滴入氨水,保持10min时间后过滤洗涤,滤出的固体在120℃的温度条件下干燥得到碱式碳酸镁产品.
碱式碳酸镁密度小,是橡胶制品的优良填料.可用复盐MgCO3•(NH4)2CO3•H2O作原料制各.取一定量的含镁复盐放三颈烧瓶中,并将三颈烧瓶放在恒温水浴锅中加热(如图1所示),按一定的液固比加入蒸馏水,开启搅拌器同时加入预定的氨水,待温度到达40℃时开始热解,此时滴加卤水(氯化镁溶液)并继续滴入氨水,保持10min时间后过滤洗涤,滤出的固体在120℃的温度条件下干燥得到碱式碳酸镁产品.
(1)本实验选择水浴加热方式,其优点是使反应物受热均匀,温度容易控制.
(2)40℃时复盐开始热解生成MgCO3•3H2O,并有气体产生,该反应的化学方程式为MgCO3•(NH4)2CO3•H2O+H2O$\frac{\underline{\;\;△\;\;}}{\;}$MgCO3•3H2O+2NH3↑+CO2↑.
(3)碱式碳酸镁产品中镁的质量分数[w(Mg)%]越高,产品质最越好,氯的质量分数越高,产品质量越差.某科研小组用沉淀滴定法分析产品中C1-的含量,称取6.1000g产品用适量硝酸溶解,经稀释等步骤最终配得500mL的溶液.①在配制过程中必需要用到的一种计量仪器是电子天平或分析天平.准确最取25.00mL待测液,用硝酸银标准液进行滴定,滴定前后滴定管中的液面读数如图2所示,则滴定过程中消耗标准液的体积为16mL.
②已知某温度时,一些银盐的颜色和Ksp如下表:
则滴定时,可用作指示剂的是d.
a.CaCl2b.NaBr c.NaI d.K2CrO4
③滴定时,应将溶液调成中性,不能是强酸性或强碱性,其中不能是强碱性的原因是碱性条件下,硝酸银会生成氢氧化银或氧化银沉淀.
(4)已知制得的碱式碳酸镁可表示为xMgC03′yMg(OH)2H2O.若碱式碳酸镁的质量ag(不考虑微最杂质),充分灼烧后,测得剩余固体的质量为bg,产生的二氧他碳气体体积在标准状况下为cL,则碱式碳酸镁中x:y=40c:(22.4b-40c).(用b、c表示,不需化简)
 碱式碳酸镁密度小,是橡胶制品的优良填料.可用复盐MgCO3•(NH4)2CO3•H2O作原料制各.取一定量的含镁复盐放三颈烧瓶中,并将三颈烧瓶放在恒温水浴锅中加热(如图1所示),按一定的液固比加入蒸馏水,开启搅拌器同时加入预定的氨水,待温度到达40℃时开始热解,此时滴加卤水(氯化镁溶液)并继续滴入氨水,保持10min时间后过滤洗涤,滤出的固体在120℃的温度条件下干燥得到碱式碳酸镁产品.
碱式碳酸镁密度小,是橡胶制品的优良填料.可用复盐MgCO3•(NH4)2CO3•H2O作原料制各.取一定量的含镁复盐放三颈烧瓶中,并将三颈烧瓶放在恒温水浴锅中加热(如图1所示),按一定的液固比加入蒸馏水,开启搅拌器同时加入预定的氨水,待温度到达40℃时开始热解,此时滴加卤水(氯化镁溶液)并继续滴入氨水,保持10min时间后过滤洗涤,滤出的固体在120℃的温度条件下干燥得到碱式碳酸镁产品.(1)本实验选择水浴加热方式,其优点是使反应物受热均匀,温度容易控制.
(2)40℃时复盐开始热解生成MgCO3•3H2O,并有气体产生,该反应的化学方程式为MgCO3•(NH4)2CO3•H2O+H2O$\frac{\underline{\;\;△\;\;}}{\;}$MgCO3•3H2O+2NH3↑+CO2↑.
(3)碱式碳酸镁产品中镁的质量分数[w(Mg)%]越高,产品质最越好,氯的质量分数越高,产品质量越差.某科研小组用沉淀滴定法分析产品中C1-的含量,称取6.1000g产品用适量硝酸溶解,经稀释等步骤最终配得500mL的溶液.①在配制过程中必需要用到的一种计量仪器是电子天平或分析天平.准确最取25.00mL待测液,用硝酸银标准液进行滴定,滴定前后滴定管中的液面读数如图2所示,则滴定过程中消耗标准液的体积为16mL.
②已知某温度时,一些银盐的颜色和Ksp如下表:
| 难溶盐 | AgCl | AgBr | AgI | Ag2CrO4 |
| Ksp | 2×10-10 | 5.4×10-13 | 8.3×10-17 | 2×10-12 |
| 颜色 | 白色 | 淡黄色 | 黄色 | 砖红色 |
a.CaCl2b.NaBr c.NaI d.K2CrO4
③滴定时,应将溶液调成中性,不能是强酸性或强碱性,其中不能是强碱性的原因是碱性条件下,硝酸银会生成氢氧化银或氧化银沉淀.
(4)已知制得的碱式碳酸镁可表示为xMgC03′yMg(OH)2H2O.若碱式碳酸镁的质量ag(不考虑微最杂质),充分灼烧后,测得剩余固体的质量为bg,产生的二氧他碳气体体积在标准状况下为cL,则碱式碳酸镁中x:y=40c:(22.4b-40c).(用b、c表示,不需化简)
2.设NA 为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,1.12 L CCl4含有C-Cl键的数目为0.2NA | |
| B. | 1 L 1 mol/L AlCl3溶液中含有NA个Al3+ | |
| C. | 常温常压下,4.4 g CO2与N2O的混合气体中含有的原子总数为0.3NA | |
| D. | 80 mL 10 mol•L-1盐酸与足量MnO2加热反应,产生的Cl2分子数为0.2NA |
3.同温同压下,下列各热化学方程式中热量数值最小的是( )
| A. | 2A(l)+B(l)═2C(g);△H=+Q1 | B. | 2A(g)+B(g)═2C(g);△H=+Q2 | ||
| C. | 2A(g)+B(g)═2C(l);△H=+Q3 | D. | 2A(l)+B(l)═2C(l);△H=+Q4 |