题目内容
20.高炉炼铁中发生的基本反应之一如下:FeO(s)+CO(g)?Fe(s)+CO2(g)△H>0其平衡常数可表达为K=$\frac{c(C{O}_{2})}{c(CO)}$,已知1100℃时,K=0.263.(1)温度升高,化学平衡移动后达到新的平衡,高炉内CO2和CO体积比值增大,平衡常数K值增大(均填“增大”、“减小”或“不变”).
(2)1100℃时测得高炉中,c(CO2)=0.025mol/L,c(CO)=0.1mol/L,在这种情况下,该反应是否处于化学平衡状态否(选“是”或“否”).
(3)若加入催化剂,平衡时气体混合物的总物质的量不变 (“增大”、“减小”或“不变”).
(4)向体积为2VL的密闭容器中充入6molN2和6molH2,一定条件下发生反应N2+3H2?2NH3,达到平衡时测得H2的转化率为50%.若达到平衡后将容器体积变为VL,下列说法中一定能证明再次达到平衡状态的标志是①④⑤⑥(填编号)
①H2的体积分数不再变化;
②颜色不再变化;
③气体密度不再变化;
④气体的平均分子量不再变化;
⑤温度不再变化;
⑥N2的体积分数不再变化.
分析 (1)升高温度平衡向吸热方向移动,根据平衡移动的方向判断高炉内CO2和CO的体积比值变化以及平衡常数K值;
(2)计算浓度商,与平衡常数比较,可判断反应是否达到平衡状态;
(3)催化剂对化学平衡移动没有影响;
(4)可逆反应达到平衡状态时,正逆反应速率相等,各组分的浓度不变,据此分析.
解答 解:(1)反应吸热,升高温度平衡向正反应方向移动,则高炉内CO2和CO体积比值增大,平衡常数K值增大,故答案为:增大;增大;
(2)(CO2)=0.025mol/L,c(CO)=0.1mol/L,Q=$\frac{0.025}{0.1}$=0.25<0.263,该反应不处于化学平衡状态,故答案为:否;
(3)催化剂对化学平衡移动没有影响,所以若加入催化剂,平衡时气体混合物的总物质的量不变,故答案为:不变;
(4)合成氨是气体体积减小的放热反应,
①H2的体积分数不再变化,说明各组分浓度不变,反应达到平衡状态,故正确;
②所有气体都没有颜色,所以颜色不再变化不能说明反应达到平衡状态,故错误;
③容器体积不变,气体质量不变,所以气体密度始终不变,密度不变不能说明反应达到平衡状态,故错误;
④气体的平均分子量不再变化,说明反应达到平衡状态,故正确;
⑤反应放热,温度不再变化,说明反应达到平衡状态,故正确;
⑥N2的体积分数不再变化,说明各组分浓度不变,反应达到平衡状态,故正确;
故答案为:①④⑤⑥.
点评 本题主要考查了化学平衡移动、平衡常数、化学平衡状态的判断,可以根据所学知识进行回答,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
8.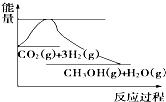 实现“节能减排”和“低碳经济”的一项重要课题就是如何将CO2转化为可利用的资源.目前工业方法是用CO2来生产燃料甲醇.一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),下图表示该反应过程中能量(单位为kJ•mol-1)的变化:关于该反应的下列说法中,正确的是( )
实现“节能减排”和“低碳经济”的一项重要课题就是如何将CO2转化为可利用的资源.目前工业方法是用CO2来生产燃料甲醇.一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),下图表示该反应过程中能量(单位为kJ•mol-1)的变化:关于该反应的下列说法中,正确的是( )
 实现“节能减排”和“低碳经济”的一项重要课题就是如何将CO2转化为可利用的资源.目前工业方法是用CO2来生产燃料甲醇.一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),下图表示该反应过程中能量(单位为kJ•mol-1)的变化:关于该反应的下列说法中,正确的是( )
实现“节能减排”和“低碳经济”的一项重要课题就是如何将CO2转化为可利用的资源.目前工业方法是用CO2来生产燃料甲醇.一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),下图表示该反应过程中能量(单位为kJ•mol-1)的变化:关于该反应的下列说法中,正确的是( )| A. | △H<0,△S<0 | B. | △H>0,△S<0 | C. | △H>0,△S>0 | D. | △H<0,△S>0 |
15.各组性质比较的表示中,正确的是( )
| A. | 沸点:Cl2<2<Br2<I2 | B. | 沸点:HF<HCl<HBr<HI | ||
| C. | 氧化性:F2<Cl2<Br2<I2 | D. | 还原性:HF<HCl<HBr<HI |
5.下列反应的离子方程式正确的是( )
| A. | Fe与稀H2SO4反应:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 硫酸铜溶液与氢氧化钡溶液反应:Ba2++SO42-═BaSO4↓ | |
| C. | 氧化铜溶于硫酸:O2-+2H+═H2O | |
| D. | NaCl溶液与AgNO3溶液反应:Ag++Cl-═AgCl↓ |
12.已知:C(s)+CO2(g)?2CO(g)△H>0.当反应达到平衡时,下列措施:
①升温 ②恒容通入惰性气体 ③增加CO2的浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体⑦增加Fe的物质的量,能提高CO2转化率的是( )
①升温 ②恒容通入惰性气体 ③增加CO2的浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体⑦增加Fe的物质的量,能提高CO2转化率的是( )
| A. | ①②⑦ | B. | ②③⑤ | C. | ①④⑥ | D. | ③⑤⑥ |
9.下列说法正确的是( )
①江河入海口三角洲的形成通常与胶体的性质有关
②“钡餐”中使用的硫酸钡是弱电解质
③冰和干冰既是纯净物又是化合物
④雾是气溶胶,在阳光下可观察到丁达尔现象
⑤某无色溶液中加入稀盐酸,产生的气体可使澄清石灰水变浑浊,则原溶液中一定含CO${\;}_{3}^{2-}$
⑥可用渗析法分离Fe(OH)3胶体和KCl溶液.
①江河入海口三角洲的形成通常与胶体的性质有关
②“钡餐”中使用的硫酸钡是弱电解质
③冰和干冰既是纯净物又是化合物
④雾是气溶胶,在阳光下可观察到丁达尔现象
⑤某无色溶液中加入稀盐酸,产生的气体可使澄清石灰水变浑浊,则原溶液中一定含CO${\;}_{3}^{2-}$
⑥可用渗析法分离Fe(OH)3胶体和KCl溶液.
| A. | ①③④⑤ | B. | ①③④⑥ | C. | ①③④⑤⑥ | D. | ①②③④⑤⑥ |
10.下列关于二氧化硫的说法正确的是( )
| A. | 二氧化硫是无色无味无毒的气体 | B. | 二氧化硫不是形成酸雨的主要成分 | ||
| C. | 二氧化硫可以与水反应形成硫酸 | D. | 二氧化硫可以使品红褪色 |
