题目内容
【题目】利用右图装置测定中和热的实验步骤如下: 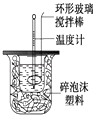
①用量筒量取50mL 0.25mol/L硫酸倒入小烧杯中,并测出其温度;
②用另一量筒量取50mL 0.55mol/L NaOH溶液,并测出其温度;
③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测出混合液最高温度.
回答下列问题:
(1)写出稀硫酸和稀氢氧化钠溶液反应的中和热的热化学方程式(中和热数值为57.3kJ/mol): .
(2)倒入NaOH溶液的正确操作是 .
A.沿玻璃棒缓慢倒入
B.分三次少量倒入
C.一次迅速倒入
(3)实验数据如表:
①请填写下表中的空白:
温度 | 起始温 | 终止温度t2/℃ | 温度差平均值 | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 29.5 | |
3 | 25.9 | 25.9 | 25.9 | 29.2 | |
3 | 26.4 | 26.2 | 26.3 | 29.8 | |
②近似认为0.55mol/L NaOH溶液和0.25mol/L硫酸溶液的密度都是1g/cm3 , 中和后生成溶液的比热容c=4.18J/(g℃).则中和热△H=( 保留一位小数).
【答案】
(1)NaOH(aq)+ ![]() ?H2SO4(aq)=
?H2SO4(aq)= ![]() ?Na2SO4(aq)+H2O(l)△H=﹣57.3kJ/mol
?Na2SO4(aq)+H2O(l)△H=﹣57.3kJ/mol
(2)C
(3)3.4℃;﹣56.8kJ/mol
【解析】解:(1.)中和热数值为57.3kJ/mol,反应放热,则中和热的热化学方程式:NaOH(aq)+ ![]() H2SO4(aq)=
H2SO4(aq)= ![]() Na2SO4(aq)+H2O(l)△H=﹣57.3kJ/mol;所以答案是:NaOH(aq)+
Na2SO4(aq)+H2O(l)△H=﹣57.3kJ/mol;所以答案是:NaOH(aq)+ ![]() H2SO4(aq)=
H2SO4(aq)= ![]() Na2SO4(aq)+H2O(l)△H=﹣57.3kJ/mol;
Na2SO4(aq)+H2O(l)△H=﹣57.3kJ/mol;
(2.)倒入氢氧化钠溶液时,必须一次迅速的倒入,目的是减少热量的散失,不能分几次倒入氢氧化钠溶液,否则会导致热量散失,影响测定结果,
所以答案是:C;
(3.)3次温度差分别为:3.4℃,3.3℃,3.5℃,3组数据均有效,温度差平均值3.4℃,50mL 0.25mol/L硫酸与50mL 0.55mol/L NaOH溶液进行中和反应生成水的物质的量为0.05L×0.25mol/L×2=0.025mol,溶液的质量为100ml×1g/ml=100g,温度变化的值为△T=3.4℃,则生成0.025mol水放出的热量为Q=mc△T=100g×4.18J/(g℃)×3.4℃=1421.2J,即1.4212KJ,所以实验测得的中和热△H=﹣ ![]() =﹣56.8kJ/mol;所以答案是:3.4℃;﹣56.8kJ/mol.
=﹣56.8kJ/mol;所以答案是:3.4℃;﹣56.8kJ/mol.

【题目】(1)某温度时,在3L密闭容器中进行的某一可逆反应,该反应中的X、Y、Z三种物质的物质的量随时间变化的曲线如下图所示。由图中数据分析:

①该反应的化学方程式:______________________。
②反应开始至3min末,Z的反应速率为_____________________。
③该反应是由_____________开始反应的。(填“正反应”、“逆反应”或“正、逆反应同时”)
(2)将SO2、O2在某密闭容器中混合,在450 ℃发生反应:2SO2(g)+O2(g) ![]() SO3(g)。
SO3(g)。
①增大压强,则正反应速率________(填:增大、减小或不变,下同),逆反应速率________。
②维持容器容积不变,加入0.1 mol SO2的一瞬间,正反应速率________,逆反应速率________;若加入的是0.1 mol He,则正、逆反应速率________。
③若维持容器压强不变,加入0.1 mol He后,容器的容积________,物质的浓度________,反应速率________。
(3)在100℃时,将0.100mol N2O4气体充入1L恒容抽空的密闭容器中,隔一定时间对该容器内物质的浓度进行分析得到如表数据:
时间(s) | 0 | 20 | 40 | 60 | 80 |
c(N2O4)/mol·L-1 | 0.100 | c1 | 0.050 | c3 | c4 |
c(NO2)/mol·L-1 | 0.000 | 0.060 | c2 | 0.120 | 0.120 |
①该反应的平衡常数表达式为___________;从表中分析:c1___________c2, c3___________c4(填“>”、“<”或“=”)。
②在上述条件下,从反应开始直至达到化学平衡时,N2O4的平均反应速率为________mol·L-1·s-1
③若在相同条件下,起始时只充入0.080 mol NO2气体,则达到平衡时NO2气体的转化率为_________。





