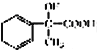题目内容
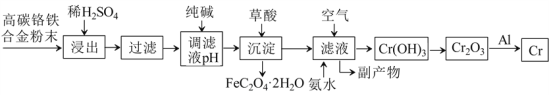
【题目】钛冶炼厂与氯碱厂、甲醇厂组成一个产业链(如图所示),将大大提高资源的利用率,减少环境污染。

请回答下列问题:
(1)Fe位于元素周期表中的位置是__________。
(2)写出流程中电解池里发生反应的离子方程式: __________。
(3)写出流程中“氯化”的化学方程式: __________。
(4)写出TiCl4完全水解生成TiO2·H2O的化学方程式: __________。
(5)高温炉中通入Ar的作用是___________。
(6)上述流程中可循环利用的物质有__________。
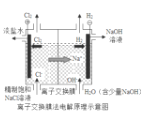
(7)下图为氯碱工业的装置示意图,使用______(填“阴”或“阳”)离子交换膜,目的除了降低分离氢氧化钠的成本外还可以________。
【答案】第四周期VIII族2Cl-+2H2O![]() Cl2↑+H2↑+2OH-2FeTiO3+6C+7Cl2
Cl2↑+H2↑+2OH-2FeTiO3+6C+7Cl2![]() 2FeCl3+2TiCl4+6COTiCl4+3H2O=TiO2·H2O+4HCl做保护气的作用,防止高温条件下Mg和Ti被氧化Mg和C l2阳防止氯气与氢氧化钠溶液发生副反应
2FeCl3+2TiCl4+6COTiCl4+3H2O=TiO2·H2O+4HCl做保护气的作用,防止高温条件下Mg和Ti被氧化Mg和C l2阳防止氯气与氢氧化钠溶液发生副反应
【解析】
(1)Fe的原子序数为26,其最外层电子数为2,有4个电子层,原子核外电子排布为1s22s22p63s23p63d64s2,故处于第四周期第VIII族;
(2)流程中电解池里电解饱和食盐水生成氢氧化钠、氢气和氯气,发生反应的离子方程式为: 2Cl-+2H2O![]() Cl2↑+H2↑+2OH-;
Cl2↑+H2↑+2OH-;
(3) 钛铁矿在高温下与焦炭经氯化得到四氯化钛,还生成氯化铁、CO,流程中“氯化”的化学方程式为: 2FeTiO3+6C+7Cl2![]() 2FeCl3+2TiCl4+6CO ;
2FeCl3+2TiCl4+6CO ;
(4) TiCl4水解生成TiO2xH2O,同时生成HCl,水解方程式为:TiCl4+3H2O=TiO2·H2O+4HCl;
(5)高温炉中通入Ar的作用是做保护气的作用,防止高温条件下Mg和Ti被氧化;
(6)上述流程中电解熔融氯化镁得到的镁和氯气在反应中为反应原料,故可循环利用的物质有Mg和Cl2;
(7)下图为氯碱工业的装置示意图,使用阳离子交换膜只允许钠离子等阳离子通过,目的除了降低分离氢氧化钠的成本外还可以防止氯气与氢氧化钠溶液发生副反应。

 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案