题目内容
2.Al2S3只能用干法制备而不能用湿法制备,其原因是(用方程式表示)Al2S3+6H2O=2Al(OH)3↓+3H2S↑.分析 Al2S3是弱酸弱碱盐,与水发生双水解反应,据此分析.
解答 解:Al2S3是弱酸弱碱盐,与水发生双水解反应,其反应为:Al2S3+6H2O=2Al(OH)3↓+3H2S↑,所以Al2S3固体的制备过程中不能有水;
故答案为:Al2S3+6H2O=2Al(OH)3↓+3H2S↑.
点评 本题考查了盐的双水解等,注意把握题干中的信息是解决本题的关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.2SO2+O2?2SO3△H<0是工业上接触法制硫酸的重要反应.下列关于该反应的说法不正确的是( )
| A. | 增加O2的浓度提高SO2的转化率 | |
| B. | 利用该反应放出的热量对SO2、O2预热 | |
| C. | 降低温度能加快反应的速率 | |
| D. | 即使增大压强也不能使SO2全部转化为SO3 |
13.下列化学用语表述正确的是( )
| A. | HCl的电子式: | B. | 乙烯的比例模型: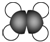 | ||
| C. | 明矾的化学式:KAl(SO4)2 | D. | 间-硝基甲苯的结构简式: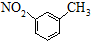 |
7.${\;}_{\;}^{37}$Cl、${\;}_{\;}^{35}$Cl为不同的核素,下列说法正确的是( )
| A. | ${\;}_{\;}^{37}$Cl2的摩尔质量是74 | |
| B. | 通常情况下,氯气做氧化剂,但氯气也具有还原性 | |
| C. | 35克的${\;}_{\;}^{35}$Cl2含有电子17mol | |
| D. | 常温下,4.48L ${\;}_{\;}^{37}$Cl2含有8NA 个中子(NA 为阿伏加德罗常数) |
14.X、Y、Z、W、R属于短周期主族元素,X在短周期主族元素中原子半径最大,Y元素的原子最外层电子数为m,次外层电子数为n,Z元素的原子L层电子数为m+n,M层电子数为m-n,W元素与Z元素同主族,R元素原子与Y元素原子的核外电子数之比为2:1.下列叙述正确的是( )
| A. | 原子半径:X>R>Z>Y | |
| B. | 最高价氧化物对应水化物的酸性:R>Z>W | |
| C. | 对应单质的沸点:X>Z>Y | |
| D. | RY2、WY2通入BaCl2溶液中均无白色沉淀生成 |
11.用一种阴、阳离子双隔膜三室电解槽处理废水中的NH4+,模拟装置如图所示,下列说法正确的是( )
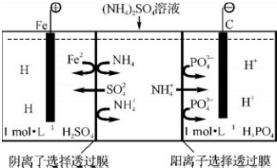

| A. | 阳极室溶液由无色变成棕黄色 | |
| B. | 阴极的电极反应式为:4OH--4e═2H2O+O2↑ | |
| C. | 电解一段时间后,阴极室溶液中的pH升高 | |
| D. | 电解一段时间后,阴极室溶液中的溶质一定是(NH4)3PO4 |
14.下列离子方程式中正确的是( )
| A. | 稀醋酸与NaOH溶液的反应:H++OH-═H2O | |
| B. | 铜粉与稀硝酸的反应:Cu+2H+═Cu2++H2↑ | |
| C. | 氯气与碘化钾溶液的反应:Cl2+I-═Cl-+I2 | |
| D. | 碳酸钠溶液与足量稀盐酸的反应:CO32-+2H+═CO2↑+H2O |
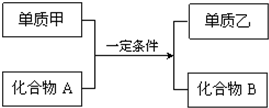 置换反应的通式可表示为:
置换反应的通式可表示为: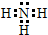 ;
;