题目内容
13.下列化学用语表述正确的是( )| A. | HCl的电子式: | B. | 乙烯的比例模型: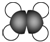 | ||
| C. | 明矾的化学式:KAl(SO4)2 | D. | 间-硝基甲苯的结构简式: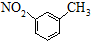 |
分析 A.氯化氢为共价化合物,分子中不存在阴阳离子;
B.乙烯为平面结构,碳原子的相对体积大于氢原子;
C.明矾为十二水合硫酸铝钾,该化学式中缺少12个结晶水;
D.硝基的表示方法不规范,正确表示为:O2N-.
解答 解:A.氯化氢属于共价化合物,分子中存在氢氯键,氯化氢正确的电子式为: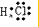 ,故A错误;
,故A错误;
B.乙烯分子中存在碳碳双键,为平面结构,乙烯的比例模型为: ,故B正确;
,故B正确;
C.明矾正确的化学式为:KAl(SO4)2•12H2O,故C错误;
D.硝基的表示方法错误,间-硝基甲苯正确的结构简式: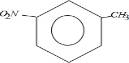 ,故D错误;
,故D错误;
故选B.
点评 本题考查了电子式、结构简式、比例模型、化学式的表示方法判断,题目难度中等,注意掌握常见化学用语的概念及表示方法,D为易错点,需要明确硝基的正确表示方法.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
3.等物质的量浓度的下列五种溶液:①CH3COOH ②(NH4)2CO3③NaHSO4 ④Ba(OH)2,溶液中水的电离程度由大到小排列是( )
| A. | ②>①>③>④ | B. | ①>③>④>② | C. | ②>③>①>④ | D. | ②>③>④>① |
1.下列有关实验的叙述合理的是( )
| A. | 可用瓷坩埚灼烧氢氧化钠固体 | |
| B. | 中和热测定实验中可用铜制搅拌棒代替玻璃环形搅拌棒 | |
| C. | 用酸式滴定管量取12.00mL高锰酸钾溶液 | |
| D. | 用pH试纸测定溶液pH时先润湿,测得溶液的pH都偏小 |
8.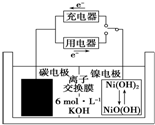 一种碳纳米管能够吸附氢气,可作二次电池(如图所示)的碳电极.该电池的电解质溶液为6mol•L-1的KOH溶液,下列说法正确的是( )
一种碳纳米管能够吸附氢气,可作二次电池(如图所示)的碳电极.该电池的电解质溶液为6mol•L-1的KOH溶液,下列说法正确的是( )
 一种碳纳米管能够吸附氢气,可作二次电池(如图所示)的碳电极.该电池的电解质溶液为6mol•L-1的KOH溶液,下列说法正确的是( )
一种碳纳米管能够吸附氢气,可作二次电池(如图所示)的碳电极.该电池的电解质溶液为6mol•L-1的KOH溶液,下列说法正确的是( )| A. | 充电时阴极发生氧化反应 | |
| B. | 充电时将碳电极与电源的正极相连 | |
| C. | 放电时碳电极反应为H2-2e-═2H+ | |
| D. | 放电时镍电极反应为NiO(OH)+H2O+e-═Ni(OH)2+OH- |
18.如表所示的五种元素中,W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22.下列说法正确的是( )
| X | Y | ||
| W | Z |
| A. | X、Y、Z三种元素最低价氢化物的沸点依次升高 | |
| B. | 由X、Y和氢三种元素形成的化合物中只有共价键 | |
| C. | 物质WY2、W3X4、WZ4均有熔点高、硬度大的特性 | |
| D. | X的阴离子比Y的阴离子离子半径大 |
5.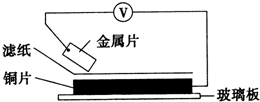 将洁净的金属片甲、乙、丙、丁分别放置在浸有某种盐溶液的滤纸上面并压紧(如图所示).在每次实验时,记录电压指针的移动方向和电压表的读数如下表:(已知构成两电极的金属其金属活泼性相差越大,电压表的读数越大.)依据记录数据判断,下列结论中正确的是( )
将洁净的金属片甲、乙、丙、丁分别放置在浸有某种盐溶液的滤纸上面并压紧(如图所示).在每次实验时,记录电压指针的移动方向和电压表的读数如下表:(已知构成两电极的金属其金属活泼性相差越大,电压表的读数越大.)依据记录数据判断,下列结论中正确的是( )
 将洁净的金属片甲、乙、丙、丁分别放置在浸有某种盐溶液的滤纸上面并压紧(如图所示).在每次实验时,记录电压指针的移动方向和电压表的读数如下表:(已知构成两电极的金属其金属活泼性相差越大,电压表的读数越大.)依据记录数据判断,下列结论中正确的是( )
将洁净的金属片甲、乙、丙、丁分别放置在浸有某种盐溶液的滤纸上面并压紧(如图所示).在每次实验时,记录电压指针的移动方向和电压表的读数如下表:(已知构成两电极的金属其金属活泼性相差越大,电压表的读数越大.)依据记录数据判断,下列结论中正确的是( ) | 金属 | 电子流动方向 | 电压(V) |
| 甲 | 甲→Cu | +0.78 |
| 乙 | Cu→乙 | -0.15 |
| 丙 | 丙→Cu | +1.35 |
| 丁 | E→Cu | +0.30 |
| A. | 金属乙能从硫酸铜溶液中置换出铜 | |
| B. | 甲、乙形成合金时,将该合金露置在空气中,甲先被腐蚀 | |
| C. | 在四种金属中乙的还原性最强 | |
| D. | 甲、丁若形成原电池时,甲为正极 |