题目内容
4.随着科学技术的进步,人们研制了多种甲醇质子交换膜燃料电池,以满足不同的需求.(1)如图是某笔记本电脑用甲醇质子交换膜燃料电池的结构示意图.
甲醇在催化剂作用下提供质子和电子,电子经外电路、质子经内电路到达另一极与氧气反应,电池总反应为:2CH3OH+3O2═2CO2+4H2O.则c电极是负极(填“正极”或“负极”),c电极上发生的电极反应式是2CH3OH+2H2O-12e-═2CO2+12H+.
(2)将上述甲醇质子交换膜燃料电池连接惰性电极电解足量的硫酸铜溶液,电解的总反应方程式为2CuSO4+2H2O$\frac{\underline{\;通电\;}}{\;}$2Cu+O2↑+2H2SO4,
(3)通电一段时间后,某电极质量增加1.92g,则燃料电池中消耗的甲醇质量为0.32g,
(4)若要将硫酸铜溶液恢复到电解前的浓度,可加入什么物质?CuO或CuCO3.
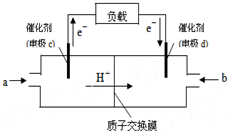
分析 (1)所有燃料电池中,通入燃料的电极是负极、通入氧化剂的电极是正极,负极上失电子、正极上得电子,放电时电子从负极沿导线流向正极,根据图知,c是负极、d是正极,电解质溶液呈酸性,所以负极上甲醇失电子和水反应生成二氧化碳和氢离子;
(2)用惰性电极电解硫酸铜溶液,阳极上氢氧根离子放电生成氧气、阴极上铜离子放电生成Cu,同时电解质溶液中还生成硫酸;
(3)通电一段时间后,某电极质量增加1.92g,该电极是阴极,析出的是Cu单质,n(Cu)=$\frac{1.92g}{64g/mol}$=0.03mol,根据转移电子相等计算消耗甲醇质量;
(4)要使电解后的溶液恢复原状,采用“析出什么加入什么”原则确定加入物质.
解答 解:(1)所有燃料电池中,通入燃料的电极是负极、通入氧化剂的电极是正极,负极上失电子、正极上得电子,放电时电子从负极沿导线流向正极,根据图知,c是负极、d是正极,电解质溶液呈酸性,所以负极上甲醇失电子和水反应生成二氧化碳和氢离子,电极反应式为2CH3OH+2H2O-12e-═2CO2+12 H+,
故答案为:负极;2CH3OH+2H2O-12e-═2CO2+12H+;
(2)用惰性电极电解硫酸铜溶液,阳极上氢氧根离子放电生成氧气、阴极上铜离子放电生成Cu,同时电解质溶液中还生成硫酸,电池反应式为2CuSO4+2H2O$\frac{\underline{\;通电\;}}{\;}$2Cu+O2↑+2H2SO4,故答案为:2CuSO4+2H2O$\frac{\underline{\;通电\;}}{\;}$2Cu+O2↑+2H2SO4;
(3)通电一段时间后,某电极质量增加1.92g,该电极是阴极,析出的是Cu单质,n(Cu)=$\frac{1.92g}{64g/mol}$=0.03mol,根据转移电子相等计算消耗甲醇质量=$\frac{0.03mol×2}{6}×32g/mol$=0.32g,故答案为:0.32g;
(4)要使电解后的溶液恢复原状,采用“析出什么加入什么”原则确定加入物质,电解硫酸铜溶液时,阳极上析出氧气、阴极上析出Cu,所以相当于析出CuO,还可以加入碳酸铜,因为碳酸铜和稀硫酸反应生成硫酸铜和二氧化碳、水,所以还相当于加入CuO,要使溶液恢复原状可以加入CuO或CuCO3,故答案为:CuO或CuCO3.
点评 本题考查化学电源新型电池、电解原理等知识点,为高频考点,侧重考查学生分析计算能力,明确各个电极上发生的反应是解本题关键,难点是电极反应式的书写,要结合电解质溶液酸碱性书写,注意(4)中加入物质确定方法,为易错点.

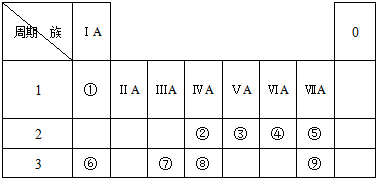
(1)②是C.
(2)9种元素中非金属性最强的是F.
(3)④⑥⑦的原子半径由小到大的顺序为O<Al<Na.
(4)②③⑧的最高价含氧酸的酸性由弱到强的顺序是H2SiO3<H2CO3<HNO3.
(5)由以上某些元素组成的有机化合物
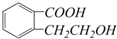 ,其分子式是C9H10O3,含氧官能团的名称是:羧基、醇羟基.
,其分子式是C9H10O3,含氧官能团的名称是:羧基、醇羟基.(6)某化学兴趣小组为探究⑨单质、Br2、Fe3+的氧化性强弱,设计了如下实验:
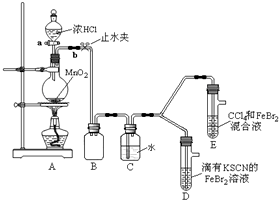
①整套实验装置存在一处明显的不足,请指出缺少尾气处理装置.
②用改正后的装置进行实验,实验过程如下:
| 实验操作 | 实验现象 | 结论 |
| 打开活塞a,向圆底烧瓶中滴入适量浓盐酸;然后关闭活塞a,点燃酒精灯. | D装置中:溶液变红 E装置中:水层溶液变黄,振荡后,CCl4层无明显变化,持续通入一段时间后,CCl4层变为棕色 | ⑨单质、Br2、Fe3+的氧化性由强到弱的顺序是: ⑨单质(或Cl2)>Br2>Fe3+ |
| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
 营养平衡、科学使用食品添加剂有助于健康和提高免疫力.
营养平衡、科学使用食品添加剂有助于健康和提高免疫力.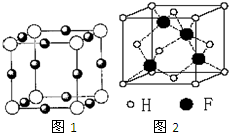 已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E<F.其中A原子核外有三个未成对电子;化合物B2E的晶体为离子晶体,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的晶体类型在同周期的单质中没有相同的;F原子核外最外层电子数与B相同,其余各层电子均充满.请根据以上信息,回答下列问题:(答题时,A、B、C、D、E、F用所对应的元素符号表示)
已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E<F.其中A原子核外有三个未成对电子;化合物B2E的晶体为离子晶体,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的晶体类型在同周期的单质中没有相同的;F原子核外最外层电子数与B相同,其余各层电子均充满.请根据以上信息,回答下列问题:(答题时,A、B、C、D、E、F用所对应的元素符号表示)