题目内容
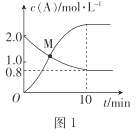
【题目】一定条件下,体积不变容器中,N2(g) + 3H2(g) ![]() 2NH3(g) ΔH=-92.4 kJ·mol-1,在反应过程中,反应速率的变化如图所示,下列说法不正确的是( )
2NH3(g) ΔH=-92.4 kJ·mol-1,在反应过程中,反应速率的变化如图所示,下列说法不正确的是( )

A. t1时刻增大c(N2)或c(H2)B. t2时刻加入催化剂
C. t3时刻降低温度D. t4时刻往容器中充入He,以增大体系压强
【答案】D
【解析】
由图象可知,t1时正反应速率突然增大,逆反应速率不变;t2时正、逆反应速率同等程度增大,t3时正、逆反应速率突然减小,t4时正、逆反应速率突然增大,结合影响化学反应速率和化学平衡的因素分析解答。
A.t1时正反应速率突然增大,逆反应速率不变,正反应速率大于逆反应速率,则平衡正向移动,应为增大反应物浓度,故A正确;
B.t2时正、逆反应速率同等程度增大,平衡不移动,则为使用了催化剂,故B正确;
C.t3时正、逆反应速率突然减小,正反应速率大于逆反应速率,则平衡正向移动,该反应为放热反应,则为降低温度,故C正确;
D.t4时正、逆反应速率突然增大,正反应速率大于逆反应速率,则平衡正向移动,则应为增大压强,但往容器中充入He,以增大体系压强,反应物和生成物浓度不变,平衡不移动,故D错误;
故选D。

【题目】二甲醚主要用于替代汽车燃油、制氢及用于燃料电池原料。 回答下列问题
⑴二甲醚在加热条件下能发生分解:(CH3)2O(g)→CH4(g)+H2(g)+CO(g),在某温度压强下测定其动力学数据如下:
t/s | 0 | 200 | 400 | 600 | 800 |
c[(CH3)2O]/mol·L-1 | 0.01000 | 0.00916 | 0.00839 | 0.00768 | 0.00702 |
0~800s 的二甲醚平均反应速率为__________________ 。
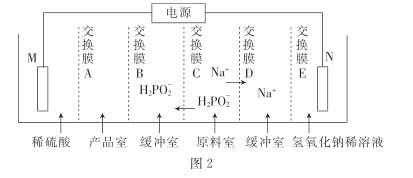
⑵一种“直接二甲醚燃料电池”结构如下图所示,电解质为强酸溶液。电池工作时,能量转化方式为______,负极的电极反应式为 ____。

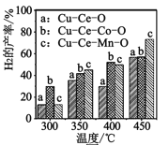
⑶二甲醚与水蒸气重整制 H2,相同投料比及流速时,单位时间内 H2 产率与催化剂及温度下关系如下图 所示,适宜的催化剂是______(选填 a、b、c)及适宜的温度是____ 。
⑷工业中用 CO 和 H2 为原料可制取二甲醚,在 250℃、5MPa 及催化剂作用下,在反应器中合成。
a:3CO(g)+3H2(g) CH3OCH3(g)+CO2(g) K1
b:2CO(g)+4H2(g) CH3OCH3(g)+H2O(g) K2
c:CO(g)+2H2(g) CH3OH(g)
已知:投料比 n(H2)/n(CO2)与原料气转化率的关系如下图 所示。
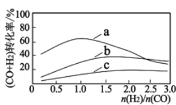
①最佳 n(H2)/n(CO)比为_________________ (填图中数字)。
②同一温度下,CO(g)+H2O(g) CO2(g)+H2(g)平衡常数为 K3,则 K3=__________用含 K1、K2 代数式表示)。
⑸已知反应 CO2(g)+3H2(g) CH3OH(g)+H2O(g)。一定条件下,向体积为 1L 的密闭容器中充入 1molCO2和 3molH2,测得 3min 时υ(H2)=0.5mol/L·min,10min 时达到平衡,平衡时,CO2 转化率为 75%,在下图中 画出 CO2 和 CH3OH(g)的浓度随时间变化曲线________。