题目内容
【题目】100mL0.50mol/L盐酸与100mL0.55mol/LNaOH溶液在图示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
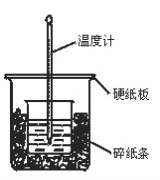
(1)从实验装置图看,尚缺少的一种玻璃仪器是________。
(2)烧杯间填充碎纸条的作用是_________。
(3)按如图装置进行实验,测得中和热的数值_______(填“偏大”“偏小”或“无影响”)其原因是_____。
(4)若实验中改用80 mL0.50mol/L盐酸跟80mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量_____(填“相等、“不相等”)。
(5)假设盐酸和氢氧化钠溶液的密度都是1g·cm-3,又知中和反应后生成溶液的比热容c=4.18J·g-1·℃-1。为了计算中和热,某学生实验记录数据如下:
实验序号 | 起始温度t1/℃ | 终止温度t2/℃ | |
盐酸 | 氢氧化钠溶液 | 混合溶液 | |
1 | 20.0 | 20.2 | 23.2 |
2 | 20.2 | 20.4 | 23.4 |
3 | 20.3 | 20.5 | 25.5 |
依据该学生测得的实验数据进行计算,中和热ΔH=______(结果保留一位小数)。
(6)能否用稀Ba(OH)2溶液和稀硫酸代替氢氧化钠溶液和盐酸反应测定中和热_______(填“能”或“否”)。
【答案】环形玻璃搅拌棒 保温隔热,减少实验过程中的热量损失 偏小 大小烧杯杯口不相平,导致热量散失较大 不相等 -51.8kJ/mol 否
【解析】
(1)为加快酸碱中和反应,用环形玻璃搅拌棒搅拌;
(2)填充泡沫或碎纸屑为减少热量损失,以免造成误差;
(3)大小烧杯口未齐平,容易造成气体对流,使热量损失过快;
(4)反应酸、碱的物质的量与原来不同,则释放的热量不同;
(5)根据表中数据,实验3数据明显偏大,舍去不用,利用实验1、2数据进行计算;
(6)Ba(OH)2与硫酸反应生成硫酸钡沉淀和水。
(1)实验中,为加快酸碱中和反应,则用环形玻璃搅拌棒进行搅拌;
(2)为减少热量损失,以免造成误差,在大小烧杯之间填充泡沫或碎纸屑进行绝热处理;
(3)按如图装置进行实验,大小烧杯口未平,容易造成气体对流,使热量损失过快,导致中和热数据偏小;
(4)用80 mL0.50mol/L盐酸跟80mL0.55mol/LNaOH溶液进行反应,酸碱的物质的量与原来不同,则释放的热量不同;
(5)根据表中数据,实验3数据明显偏大,舍去不用,则实验1、2溶液温度的平均变化值=(23.2-![]() +23.4-
+23.4-![]() )℃/2=3.1℃,Q=4.18×200×3.1 J=2591.6J,ΔH=Q/n=2.5916kJ/0.05mol=51.8kJ/mol;
)℃/2=3.1℃,Q=4.18×200×3.1 J=2591.6J,ΔH=Q/n=2.5916kJ/0.05mol=51.8kJ/mol;
(6)Ba(OH)2与硫酸反应生成硫酸钡沉淀和水,硫酸钡存在溶解平衡,使测定的中和热不准确,答案为否。

 名校课堂系列答案
名校课堂系列答案