题目内容
【题目】I.有机物A有以下一系列反应,可以转化为F,
![]()
已知E的分子式为C2H6O2,B的分子结构分析,核磁共振氢谱图中有两个峰,而且峰的面积之比为3:2。回答下列问题:
(1)A→B的反应类型是____反应,E的官能团名称是____
(2)A的结构简式为______,D的系统命名为_______
(3)写出化学方程式
①D→E___________
②B→C __________
II.某有机物的蒸气密度是相同状态下甲烷密度的5.75倍,把1.84g该有机物在氧气中充分燃烧,将生成的气体混合物通过足量碱石灰,碱石灰增重4.08g,又知生成水和二氧化碳的物质的量之比为4:3,试求此有机物的分子式为_____,已知该有机物中只含一种官能团,且两个该官能团连在同一碳上的物质不稳定,则该有机物的结构简式为___
【答案】取代 羟基 CH3CH3 1,2-二溴乙烷 BrCH2CH2Br+2NaOH![]() HOCH2CH2OH+2NaBr CH3CH2Br+NaOH
HOCH2CH2OH+2NaBr CH3CH2Br+NaOH ![]() CH2=CH2↑+NaBr+H2O C3H8O3 HOCH2CH(OH)CH2OH
CH2=CH2↑+NaBr+H2O C3H8O3 HOCH2CH(OH)CH2OH
【解析】
I.A与Br2光照下发生取代反应生成B,B与NaOH醇溶液、加热发生消去反应生成C,C与溴水发生加成反应生成D,D与NaOH溶液发生水解反应生成E,E中含—OH,E的分子式为C2H6O2,B的分子结构分析,核磁共振氢谱图中有两个峰,而且峰的面积之比为3:2,则E应为HOCH2CH2OH,D为BrCH2CH2Br,C为CH2=CH2,B为CH3CH2Br,则A为CH3CH3,E发生氧化反应生成F,以此解答该题。
II.根据相对甲烷的密度可以计算有机物的相对分子质量,碱石灰增重为燃烧生成二氧化碳、水的质量之和,结合二者物质的量之比计算各自物质的量,根据原子守恒计算有机物中C、H原子数目,再结合相对分子质量计算有机物分子中O原子数目,进而确定有机物分子式;结合有机物中只含一种官能团,且两个该官能团连在同一碳上的物质不稳定,分析结构简式。
I.(1)A为CH3CH3,B为CH3CH2Br,A在光照条件下与溴发生取代反应,生成溴乙烷,A→B的反应类型是取代反应,E为HOCH2CH2OH,E的官能团名称是羟基;
(2)A为CH3CH3,A的结构简式为CH3CH3 ,D为BrCH2CH2Br,D的系统命名为1,2-二溴乙烷;
(3)①D→E为BrCH2CH2Br的水解反应,方程式为BrCH2CH2Br+2NaOH![]() HOCH2CH2OH+2NaBr;
HOCH2CH2OH+2NaBr;
②B→C 为溴乙烷在NaOH的醇溶液中发生消去反应:CH3CH2Br+NaOH ![]() CH2=CH2↑+NaBr+H2O
CH2=CH2↑+NaBr+H2O
II.该有机物相对分子质量为16×5.75=92,1.84g该有机物物质的量为1.84g÷92g·mol-1=0.02mol,有机物燃烧生成二氧化碳、与水总质量为4.08g,且生成H2O和CO2的物质的量之比为4:3,设二者物质的量分别为4a mol、3a mol,则3a×44+4a×18=4.08,解得a=0.02,故水为0.08mol,二氧化碳为0.06mol,则有机物分子中C原子数目为0.06mol÷0.02mol=3,H原子数目为0.08mol×2÷0.02mol=8,则O原子数目为(92-12×3-8)÷16=3,故该有机物分子式为C3H8O3;
该有机物中只含一种官能团,且两个该官能团连在同一碳上的物质不稳定,说明有三个羟基平均分布在三个碳上,则该有机物的结构简式为HOCH2CH(OH)CH2OH。

 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
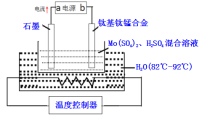
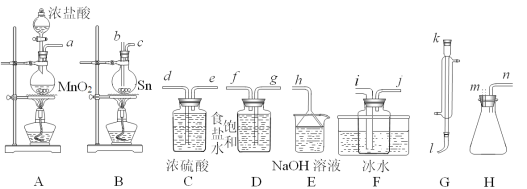
课课优能力培优100分系列答案【题目】四氯化锡(SnCl4)常作有机合成的催化剂,在空气中极易水解生成SnO2·xH2O,实验室用熔融的锡(熔点为231.9℃)与氯气反应来制备(同时有SnCl2生成),该反应是放热反应。可选用的仪器及装置如图所示。
SnCl2、SnCl4有关物理性质如表:
物质 | 颜色、状态 | 熔点/℃ | 沸点/℃ |
SnCl2 | 无色晶体 | 246 | 623 |
SnCl4 | 无色液体 | -33 | 114 |
(1)已知SnCl2、SnCl4晶体类型相同,SnCl2熔沸点高于SnCl4的原因是:___。
(2)选择装置进行连接(填各接口的字母,装置可重复使用,空格可不填满)。___
a→__,__→__,__→__,__→__,__→__,__→__,__→__,__→__。
(3)反应开始时,应先点燃装置___(填“A”或“B”,下同)的酒精灯,待___时,再点然装置___的酒精灯,并在反应进行中仍持续加热,其目的是___。
(4)该方法制得的SnCl4中含有少量SnCl2,提纯SnCl4的实验名称是___。
(5)测定产品纯度。取ag产品溶于少量浓盐酸,加入蒸馏水稀释至250mL。取20mL稀释溶液于锥形瓶,滴加几滴淀粉溶液,用cmol·L-1I2溶液滴定至终点,消耗滴定溶液V mL。
①该产品中SnCl2含量为___%。(滴定反应:Sn2++I2=Sn4++2I-,SnCl2的相对分子质量为:190)
②若操作时间过长、振荡剧烈,测得产品中SnCl4含量__(填“偏高”或“偏低”或“无影响”)。