题目内容
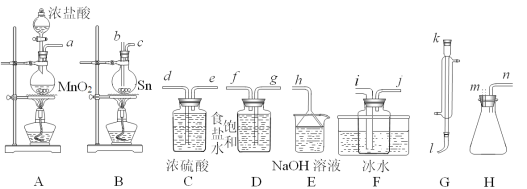
【题目】四氯化锡(SnCl4)常作有机合成的催化剂,在空气中极易水解生成SnO2·xH2O,实验室用熔融的锡(熔点为231.9℃)与氯气反应来制备(同时有SnCl2生成),该反应是放热反应。可选用的仪器及装置如图所示。
SnCl2、SnCl4有关物理性质如表:
物质 | 颜色、状态 | 熔点/℃ | 沸点/℃ |
SnCl2 | 无色晶体 | 246 | 623 |
SnCl4 | 无色液体 | -33 | 114 |
(1)已知SnCl2、SnCl4晶体类型相同,SnCl2熔沸点高于SnCl4的原因是:___。
(2)选择装置进行连接(填各接口的字母,装置可重复使用,空格可不填满)。___
a→__,__→__,__→__,__→__,__→__,__→__,__→__,__→__。
(3)反应开始时,应先点燃装置___(填“A”或“B”,下同)的酒精灯,待___时,再点然装置___的酒精灯,并在反应进行中仍持续加热,其目的是___。
(4)该方法制得的SnCl4中含有少量SnCl2,提纯SnCl4的实验名称是___。
(5)测定产品纯度。取ag产品溶于少量浓盐酸,加入蒸馏水稀释至250mL。取20mL稀释溶液于锥形瓶,滴加几滴淀粉溶液,用cmol·L-1I2溶液滴定至终点,消耗滴定溶液V mL。
①该产品中SnCl2含量为___%。(滴定反应:Sn2++I2=Sn4++2I-,SnCl2的相对分子质量为:190)
②若操作时间过长、振荡剧烈,测得产品中SnCl4含量__(填“偏高”或“偏低”或“无影响”)。
【答案】SnCl2为极性分子,SnCl4为非极性分子,SnCl2的熔沸点高于SnCl4 a→g→f→d→e→b→c→i→j→d→e→h A 装置F液面上方出现黄绿色气体 B 加快氯气与Sn的反应,且使SnCl4气化,有利于从混合物中分离出来 蒸馏 ![]() 偏高
偏高
【解析】
本题实验目的是制备SnCl4,实验原理是Sn+2Cl2![]() SnCl4,因为SnCl4易水解,因此Sn与干燥的氯气发生反应,且也要防止后续装置水蒸气的进入,因为氯气有毒,需要尾气的处理,据此分析;
SnCl4,因为SnCl4易水解,因此Sn与干燥的氯气发生反应,且也要防止后续装置水蒸气的进入,因为氯气有毒,需要尾气的处理,据此分析;
(1)SnCl2中Sn的化合价为+2价,即SnCl2为极性分子,SnCl4中Sn的化合价为+4价,即SnCl4为非极性分子,因此SnCl2的熔沸点高于SnCl4;
答案为SnCl2为极性分子,SnCl4为非极性分子,SnCl2的熔沸点高于SnCl4;
(2)根据实验目的:制备SnCl4,原理是Sn+2Cl2![]() SnCl4,装置A制备氯气,制备的氯气中含有HCl和H2O(g),Sn能与HCl反应,且SnCl4易水解,即先需要通过饱和食盐水,再通过浓硫酸进行干燥,然后将氯气通入B装置,制备SnCl4,常温下SnCl4为液体,收集装置需要放在冷水中,因为Cl2有毒,需要尾气处理,因此需要用NaOH溶液吸收,为防止NaOH溶液中水蒸气进入收集装置,需要在E装置前添加一盛有浓硫酸的洗气瓶,即连接顺序是a→g→f→d→e→b→c→i→j→d→e→h;
SnCl4,装置A制备氯气,制备的氯气中含有HCl和H2O(g),Sn能与HCl反应,且SnCl4易水解,即先需要通过饱和食盐水,再通过浓硫酸进行干燥,然后将氯气通入B装置,制备SnCl4,常温下SnCl4为液体,收集装置需要放在冷水中,因为Cl2有毒,需要尾气处理,因此需要用NaOH溶液吸收,为防止NaOH溶液中水蒸气进入收集装置,需要在E装置前添加一盛有浓硫酸的洗气瓶,即连接顺序是a→g→f→d→e→b→c→i→j→d→e→h;
答案为a→g→f→d→e→b→c→i→j→d→e→h;
(3)装置中有空气,Sn能与氧气发生反应,且SnCl4在空气中极易水解生成SnO2·xH2O,因此首先排除装置中的空气,即先点燃A处酒精灯,当观察装置F液面上方出现黄绿色气体时,表明装置中空气已排尽,开始点燃B处酒精灯;继续加热的目的是加快氯气与Sn的反应,且使SnCl4气化,有利于从混合物中分离出来;
答案为A;装置F液面上方出现黄绿色气体;B;加快氯气与Sn的反应,且使SnCl4气化,有利于从混合物中分离出来;
(4)根据表格数据,两者沸点相差过大,分离时采用蒸馏的方法;
答案为蒸馏;
(5)①根据元素守恒,n(SnCl2)=n(I2)=V×10-3L×cmol·L-1×![]() ,SnCl2含量为
,SnCl2含量为 ×100%=
×100%=![]() ;
;
②操作时间过长,可能发生4I-+O2+4H+=2I2+2H2O、2Sn2++O2+4H+=Sn4++2H2O,SnCl2消耗I2量的减少,SnCl2含量降低,则SnCl4含量偏高;
答案为![]() ;偏高。
;偏高。

【题目】已知:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O.
某化学小组根据上述反应原理进行下列实验:
I.测定H2C2O4溶液的物质的量浓度
实验步骤如下:
①取待测H2C2O4溶液25.00mL放入锥形瓶中,再加入适量的稀硫酸;
②用0.1mol/LKMnO4溶液滴定至终点,记录数据;
③重复滴定2次,平均消耗KMnO4溶液20.00mL。
请回答:
(1)滴定时,将KMnO4溶液装在______(填“酸式”或“碱式”)滴定管中。
(2)若在步骤①操作之前,先用待测H2C2O4溶液润洗锥形瓶,则测得H2C2O4溶液的浓度会______(填“偏大”“偏小”或“无影响”)。
(3)步骤②中到达滴定终点时的现象为_______________________________。
(4)计算H2C2O4溶液的物质的量浓度为__________mol/L。
II.探究反应物浓度对化学反应速率的影响设计如下实验方案(实验温度均为25℃):
实验序号 | 体积V/mL | |||
0.1molL-1KMnO4溶液 | 0.11molL-1H2C2O4溶液 | 0.11molL-1H2SO4溶液 | H2O | |
① | 2.0 | 5.0 | 6.0 | 7.0 |
② | 2.0 | 8.0 | 6.0 | V1 |
③ | 2.0 | V2 | 6.0 | 2.0 |
请回答:
(5)表中v1=______。
(6)实验中需要测量的数据是______________________________。
(7)实验中______(填“能”或“不能”)用0.2mol/L盐酸代替0.1mol/LH2SO4溶液,理由是_________。