��Ŀ����
����Ŀ����Ҫ�����ͼ���������б�Ҫ�����Ӳ���գ�

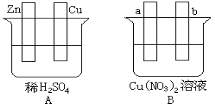
��1����Aͼ�У�ʹͭƬ��ðH2���ݡ���װ�ü������ӣ������Ӻ��װ�ý� ��
�缫��Ӧʽ��п�壺 ��ͭ�壺 ��
��2����Bͼ�У�a��b���缫��Ϊʯī����װ�ü������ӣ�ʹa������ͭ����b���� ����װ�ý� ���缫��Ӧʽ��a���� b���� ������һ��ʱ���ֹͣ��Ӧ��������Һ����Һ��pHֵ �����ߡ����͡����䣩������һ������ ���ѧʽ������Һ�ָܻ�������ǰ��ȫһ�¡�
���𰸡���1��ԭ��� Zn -2e- = Zn2+ 2H+ +2e- = H2��
��2��O2 ���� Cu2+ + 2e- = Cu 4OH- - 4e- = O2��+ 2H2O ���� CuO
��������
�����������1����Aͼ�У�ʹͭƬ��ðH2���ݣ���ͭƬ��������п����������װ������ԭ��أ�п�缫�Ϸ���������Ӧ���缫��ӦʽΪ��Zn-2e-=Zn2+��ͭ�缫�������ӷ�����ԭ��Ӧ���缫��ӦʽΪ��2H++2e-=H2����
��2����Bͼ�У�a��b���缫��Ϊʯī��ʹa������ͭ�����Ը�װ���ǵ��أ�a��������������ͭ���ӵõ��ӷ�����ԭ��Ӧ���缫��ӦʽΪ��Cu+2e-=Cu2+��b������������������������ʧ���ӷ���������Ӧ�������������缫��ӦΪ4OH- - 4e- = O2��+ 2H2O������Һ������������Ũ�ȼ�С����������Ũ�ȱ����Һ��pHֵ���ͣ����ݡ�����ʲô����ʲô����ԭ��������ʣ�����������ͭ������������������Ҫʹ��Һ�ָܻ�ԭ��״̬Ӧ�ü�������ͭ��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�