题目内容
4.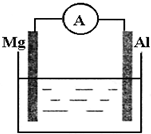 如图所示装置
如图所示装置 (1)若烧杯中溶液为稀硫酸,则两极反应式为:
负极Mg-2e-=Mg2+
正极2H++2e-=H2↑
(2)若烧杯中溶液为氢氧化钠溶液,则负极为Al(填电极材料),总反应的离子方程为2Al+2OH-+2H2O=2AlO2-+3H2↑.
分析 (1)若烧杯中溶液为稀硫酸,该装置符合原电池构成条件,所以能构成原电池,则电流表指针发生偏转,Mg易失电子作负极、Al作正极,负极反应式为Mg-2e-=Mg2+、正极反应式为2H++2e-=H2↑;
(2)若烧杯中溶液为氢氧化钠溶液,碱性条件下,Al易失电子作负极、Mg作正极,Al和NaOH、H2O反应生成NaAlO2、H2.
解答 解:(1)若烧杯中溶液为稀硫酸,该装置符合原电池构成条件,所以能构成原电池,则电流表指针发生偏转,Mg易失电子作负极、Al作正极,负极反应式为Mg-2e-=Mg2+、正极反应式为2H++2e-=H2↑,故答案为:Mg-2e-=Mg2+;2H++2e-=H2↑;
(2)若烧杯中溶液为氢氧化钠溶液,碱性条件下,Al易失电子作负极、Mg作正极,负极反应式为Al+4OH--3e-═AlO2-+2H2O,正极反应式为2H2O+2e-=H2↑+2OH-,总反应的离子方程为2Al+2OH-+2H2O=2AlO2-+3H2↑,
故答案为:Al;2Al+2OH-+2H2O=2AlO2-+3H2↑.
点评 电极反应式的书写要注意结合电解质溶液酸碱性、物质的性质,不能根据金属的活泼性强弱判断正负极,为易错点.

练习册系列答案
相关题目
14.下列物质是共价化合物的是( )
| A. | H2SO4 | B. | MgCl2 | C. | N2 | D. | NH4Cl |
16.把A、B、C、D四块金属泡在稀H2SO4中,用导线两两相连可以组成各种原电池.A、B相连时,A为负极;C、D相连时,D上有气泡逸出;A、C相连时,A极减轻;B、D相连时,B为正极.则四种金属的活动性顺序由大到小排列为( )
| A. | A>B>C>D | B. | A>C>B>D | C. | A>C>D>B | D. | B>D>C>A |
14.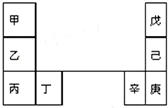 甲--辛等元素在周期表中的相对位置如图.甲和戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁和辛属同周期元素,下列判断正确的是( )
甲--辛等元素在周期表中的相对位置如图.甲和戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁和辛属同周期元素,下列判断正确的是( )
 甲--辛等元素在周期表中的相对位置如图.甲和戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁和辛属同周期元素,下列判断正确的是( )
甲--辛等元素在周期表中的相对位置如图.甲和戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁和辛属同周期元素,下列判断正确的是( )| A. | 金属性:甲>乙>丁 | |
| B. | 原子半径:辛>己>戊 | |
| C. | 丙与庚的原子核外电子数相差14 | |
| D. | 乙的单质在空气中燃烧生成只含离子键的化合物 |
 .
.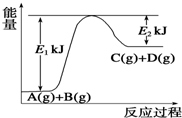 已知某反应A(g)+B(g)?C(g)+D(g),过程中的能量变化如图所示,回答下列问题.
已知某反应A(g)+B(g)?C(g)+D(g),过程中的能量变化如图所示,回答下列问题.