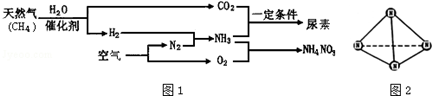
籾朕坪否
16⤴委A、B、C、D膨翠署奉倒壓蓮H2SO4嶄⇧喘擬㞍曾曾屢銭辛參怏撹光嶽圻窮学⤴A、B屢銭扮⇧A葎減自◉C、D屢銭扮⇧D貧嗤賑倒叺竃◉A、C屢銭扮⇧A自受煤◉B、D屢銭扮⇧B葎屎自⤴夸膨嶽署奉議試強來乏會喇寄欺弌電双葎↙ ⇄| A⤴ | A﹅B﹅C﹅D | B⤴ | A﹅C﹅B﹅D | C⤴ | A﹅C﹅D﹅B | D⤴ | B﹅D﹅C﹅A |
蛍裂 匯違栖傍⇧壓圻窮学嶄⇧恬減自議署奉凪署奉試強來寄噐恬屎自議署奉⇧払窮徨窟伏剳晒郡哘議署奉恬減自、誼窮徨窟伏珊圻郡哘議署奉恬屎自⇧象緩登僅署奉來膿樋乏會⤴
盾基 盾⦿匯違栖傍⇧壓圻窮学嶄⇧恬減自議署奉凪署奉試強來寄噐恬屎自議署奉⇧払窮徨窟伏剳晒郡哘議署奉恬減自、誼窮徨窟伏珊圻郡哘議署奉恬屎自⇧
A、B屢銭扮⇧A葎減自⇧夸署奉試強來乏會A﹅B◉
C、D屢銭扮⇧D貧嗤賑倒叺竃⇧傍苧D貧誼窮徨窟伏珊圻郡哘⇧夸署奉試強來C﹅D◉
A、C屢銭扮⇧A自受煤⇧傍苧A払窮徨窟伏剳晒郡哘⇧夸署奉試強來A﹅C◉
B、D屢銭扮⇧B葎屎自⇧夸署奉試強來D﹅B⇧
侭參宸叱嶽署奉試強來乏會頁A﹅C﹅D﹅B⇧絞僉C⤴
泣得 云籾參圻窮学圻尖葎墮悶深臥署奉試強來膿樋登僅⇧屎鳩登僅圻窮学屎減自頁盾云籾購囚⇧辛參功象郡哘窃侏、窮徨送﨑、窮送送﨑、窮盾嵎卑匣嶄咐剩宣徨卞強圭﨑、署奉窮自可創嵎楚延晒、誼払窮徨吉圭中登僅⇧籾朕佃業音寄⤴

膳楼過狼双基宛
 兆丕仁銘狼双基宛
兆丕仁銘狼双基宛
屢購籾朕
6⤴和双郡哘嶄⇧音奉噐剳晒珊圻郡哘議頁↙ ⇄
| A⤴ | 2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$ 2H2O+O2● | |
| B⤴ | NH4Cl$\frac{\underline{\;\;@\;\;}}{\;}$NH3●+HCl● | |
| C⤴ | 2Al+Fe2O3 $\frac{\underline{\;互梁\;}}{\;}$ 2Fe+Al2O3 | |
| D⤴ | Cu+2H2SO4↙敵⇄$\frac{\underline{\;\;@\;\;}}{\;}$CuSO4+SO2●+2H2O |
11⤴和双並糞嬬傍苧冉嵓磨頁樋窮盾嵎議頁↙ ⇄
〙25≧扮冉嵓磨墜卑匣議pH寄噐7
〖喘HNO2卑匣恂擬窮編刮⇧菊倒載圧
〗HNO2卑匣音嚥Na2SO4卑匣郡哘
∠0.1mol•L-1 HNO2卑匣議pH=2.1⤴
〙25≧扮冉嵓磨墜卑匣議pH寄噐7
〖喘HNO2卑匣恂擬窮編刮⇧菊倒載圧
〗HNO2卑匣音嚥Na2SO4卑匣郡哘
∠0.1mol•L-1 HNO2卑匣議pH=2.1⤴
| A⤴ | 〙〖〗 | B⤴ | 〖〗∠ | C⤴ | 〙∠ | D⤴ | 〙〖∠ |
5⤴辛喘匯嶽編質授艶KCl、Ba↙OH⇄2、Na2CO3、K2SO3膨嶽卑匣⇧乎編質頁↙ ⇄
| A⤴ | BaCl2 | B⤴ | H2SO4 | C⤴ | KOH | D⤴ | HCl |
6⤴和双麗嵎岻寂議廬晒⇧嬬匯化頼撹議頁↙ ⇄
| A⤴ | CH3CH2OH★CH3CHO | B⤴ | Fe2O3★Fe↙OH⇄3 | C⤴ | SiO2★H2SiO3 | D⤴ | Al2O3★Al↙OH⇄3 |
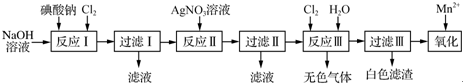
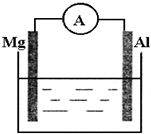 泌夕侭幣廾崔
泌夕侭幣廾崔