题目内容
【题目】下表是A、B、C、D四种有机物的有关信息:
A | ①能使溴的四氯化碳溶液褪色;②比例模型为 |
B | ①由C、H两种元素组成;②球棍模型为 |
C | ①由C、H、O三种元素组成;②能与Na反应,但不能与NaOH溶液反应;③能与D反应生成相对分子质量为88的酯 |
D | ①由C、H、O三种元素组成;②球棍模型为 |
回答下列问题:
(1)A与溴的四氯化碳溶液反应的化学方程式为:___________________。
(2)B具有的性质是________(填序号)。
①无色无味液体 ②有毒 ③不溶于水 ④密度比水大
⑤与酸性KMnO4溶液和溴水反应褪色 ⑥任何条件下不与氢气反应
(3)B在50~60℃时,能与混酸(浓硫酸和浓硝酸的混合溶液)反应,该反应的反应类型是_______________,化学方程式为___________________。
(4)C与D反应生成有香味的物质的化学方程式为: _______________,该反应的反应类型是_______________。
(5)B与液溴及铁反应的化学方程式为:__________, 生成有机物的名称是________。
【答案】 CH2=CH2+Br2→![]() ②③ 硝化反应
②③ 硝化反应 ![]() +HNO3
+HNO3 ![]()
![]() +H2O CH3COOH+CH3CH2OH
+H2O CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O 酯化反应
CH3COOCH2CH3+H2O 酯化反应 ![]() +Br2
+Br2![]()
![]() +HBr 溴苯
+HBr 溴苯
【解析】由表格中的信息可知,A为CH2=CH2,A与水加成生成C,C为CH3CH2OH,由B的球棍模型可知,B为苯,由D的球棍模型可知D为CH3COOH,C与D酯化反应生成酯为CH3COOCH2CH3,
(1)A是乙烯与溴的四氯化碳溶液发生加成反应,化学方程式为:CH2=CH2+Br2→![]() ;(2)B是苯具有的性质是苯在常温下为无色透明液体.密度(15℃)0.885克/厘米3,沸点80.10℃,熔点5.53℃,易挥发,有强烈芳香,有毒,难溶于水,易溶于乙醇、乙醚等有机溶剂。①无色芳香味液体,故错误;②有毒,正确;③不溶于水,正确;④密度比水小,错误;⑤与酸性KMnO4溶液和溴水反应褪色均不反应,错误;⑥一定条件下与氢气反应,错误;故选②③;(3)苯在50~60℃时,能与混酸(浓硫酸和浓硝酸的混合溶液)反应,该反应的反应类型是硝化反应,化学方程式为
;(2)B是苯具有的性质是苯在常温下为无色透明液体.密度(15℃)0.885克/厘米3,沸点80.10℃,熔点5.53℃,易挥发,有强烈芳香,有毒,难溶于水,易溶于乙醇、乙醚等有机溶剂。①无色芳香味液体,故错误;②有毒,正确;③不溶于水,正确;④密度比水小,错误;⑤与酸性KMnO4溶液和溴水反应褪色均不反应,错误;⑥一定条件下与氢气反应,错误;故选②③;(3)苯在50~60℃时,能与混酸(浓硫酸和浓硝酸的混合溶液)反应,该反应的反应类型是硝化反应,化学方程式为![]() +HNO3
+HNO3 ![]()
![]() +H2O ;(4) 乙醇与乙酸反应生成有香味的物质乙酸乙酯,乙醇提供-H,乙酸提供―OH,化学方程式为:CH3COOH+CH3CH2OH
+H2O ;(4) 乙醇与乙酸反应生成有香味的物质乙酸乙酯,乙醇提供-H,乙酸提供―OH,化学方程式为:CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O,该反应的反应类型是酯化反应。(5)苯与液溴及铁反应,苯环上的氢被溴原子取代,化学方程式为:
CH3COOCH2CH3+H2O,该反应的反应类型是酯化反应。(5)苯与液溴及铁反应,苯环上的氢被溴原子取代,化学方程式为: ![]() +Br2
+Br2![]()
![]() +HBr, 生成有机物的名称是溴苯
+HBr, 生成有机物的名称是溴苯

 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
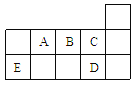
黄冈天天练口算题卡系列答案【题目】下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试回答下列问题:

(1)写出元素k的基态原子的电子排布式________________________________,其原子核外有________个未成对电子。
(2)单质c在空气中充分燃烧的产物的分子构型为________ ,中心原子的杂化方式为_______,该分子含有________(填“极性键”或“非极性键”),该分子是________分子(填“极性”或“非极性”)。
(3)上述元素的最高价氧化物的水化物中,酸性最强的是___________________,碱性最的___________________(填化学式)。(每空1分)
(4)d的气态氢化物与d的最高价氧化物的水化物反应的离子方程式是:___________________________________________________________________________________________________________________________________。
(5)o、p两元素的部分电离能数据列于下表:比较两元素的I2、I3可知,气态o2+再失去一个电子比气p2+再失去一个电子困难。对此,你的解是__________________________________________________________________________。
元素 | o | P | |
电离能/kJ·mol-1 | I1 | 717 | 759 |
I2 | 1509 | 1561 | |
I3 | 3248 | 2957 | |

(6)短周期某主族元素的电离能情况如上图所示,则元素是上述周期表的__________元素(填元素符号)。