题目内容
8.CuCl2溶液有时呈黄色,有时呈绿色或蓝色,这是因为CuCl2的水溶液中存在如下平衡:[CuCl2(H2O)4]2++4Cl-?[CuCl4]2-+4H2O.
蓝色 黄色
现欲使溶液由黄色变为绿色或蓝色,请写出两种可采用的方法加入硝酸银溶液、加水稀释.
分析 使溶液由黄色变成蓝色,应使平衡向左移动,能够使化学平衡向逆反应方向移动的措施都是可以的.
解答 解:使溶液由黄色变成绿色或蓝色,应使平衡向左移动,能够使化学平衡向逆反应方向移动的措施即可.
根据化学平衡移动原理,可以加入硝酸银溶液,使之和氯离子反应来减少氯离子的浓度,使得平衡左移;
根据化学平衡移动原理,加入水稀释,平衡向着离子数目增加的方向进行,即向着逆反应方向进行.
故答案为:加入硝酸银溶液;加水稀释.
点评 本题考查化学平衡的影响因素,难度不大,侧重对基础知识的考查,注意化学平衡移动原理的应用和掌握.

练习册系列答案
 字词句段篇系列答案
字词句段篇系列答案
相关题目
6.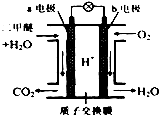 二甲醚是一种绿色、可再生的新能源.图是绿色电源“二甲醚燃料电池”的工作原理示意图(a、b均为多孔性Pt电极).该电池工作时,下列说法不正确的是( )
二甲醚是一种绿色、可再生的新能源.图是绿色电源“二甲醚燃料电池”的工作原理示意图(a、b均为多孔性Pt电极).该电池工作时,下列说法不正确的是( )
 二甲醚是一种绿色、可再生的新能源.图是绿色电源“二甲醚燃料电池”的工作原理示意图(a、b均为多孔性Pt电极).该电池工作时,下列说法不正确的是( )
二甲醚是一种绿色、可再生的新能源.图是绿色电源“二甲醚燃料电池”的工作原理示意图(a、b均为多孔性Pt电极).该电池工作时,下列说法不正确的是( )| A. | a电极为该电池负极 | |
| B. | 电池工作时,燃料电池内部H+从a电极移向b电极 | |
| C. | 电池工作时,a电极反应式:CH3OCH3-12e-+3H2O═2CO2↑+12H+ | |
| D. | O2在b电极上得电子,电极反应式:O2+4e-+2H2O═4OH- |
3.已知3.0g乙烷完全燃烧在常温下放出的热量为155.98kJ,则下列表示乙烷燃烧热的热化学方程式书写正确的是( )
| A. | 2C2H6(g)+7O2(g)═4CO2(g)+6H2O(g)△H=-2119.6kJ/mol | |
| B. | C2H6(g)+$\frac{5}{2}$O2(g)═2CO(g)+3H2O(g)△H=-1559.8kJ/mol | |
| C. | C2H6(g)+$\frac{7}{2}$O2(g)═2CO2(g)+3H2O(g)△H=-1559.8kJ/mol | |
| D. | C2H6(g)+$\frac{7}{2}$O2(g)═2CO2(g)+3H2O(l)△H=-1559.8kJ/mol |
13.设NA为阿伏加德罗常数,则下列叙述中正确的是( )
| A. | 6.02×1022个H2SO4分子在水中可电离生成2NA个H+ | |
| B. | 在0℃、101 kPa时,22.4 L氢气中含有NA个氢原子 | |
| C. | 14 g氮气中含有7NA个电子 | |
| D. | NA个一氧化碳分子和0.5 mol甲烷的质量比为7:4 |
17.硫在空气中燃烧生成气体A.把A溶于水得溶液B.向B中滴加溴水,溴水褪色,B变成C.在C里加Na2S产生气体D.把D通入B溶液得浅黄色沉淀E.按A、B、C、D、E顺序排列的是( )
| A. | SO2、H2SO4、H2SO3、H2S、S | B. | SO2、H2SO3、H2SO4、H2S、S | ||
| C. | SO2、H2SO3、H2SO4、SO3、S | D. | SO2、H2SO3、H2SO4、SO2、S |
18.标准状况下有下列对这四种气体的关系从小到大表示不正确的是( )
①6.72L甲烷 ②3.01×1023个氯化氢分子 ③13.6g硫化氢
④0.2mol NH3.
①6.72L甲烷 ②3.01×1023个氯化氢分子 ③13.6g硫化氢
④0.2mol NH3.
| A. | 体积:④<①<②<③ | B. | 密度:①<④<③<② | ||
| C. | 质量:④<①<③<② | D. | 氢原子数:②<④<③<① |

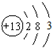 ;
;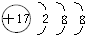 .
.