题目内容
14.下列含氧酸中,酸性最弱的是( )| A. | HClO | B. | HNO2 | C. | H2SO4 | D. | HIO4 |
分析 含氧酸可用通式XOm(OH)n来表示,式中m大于等于2的是强酸,m为0的是弱酸,据此可知,非羟基氧原子数目越大,酸性越强,将选项中含氧酸改写成XOm(OH)n形式,根据非羟基氧原子数目判断.
解答 解:A、HClO可以改写为Cl(OH)1,非羟基氧原子数目为0;
B、HNO2可以改写为NO(OH),非羟基氧原子数目为1;
C、H2SO4可以为SO2(OH)2,非羟基氧原子数目为2;
D、HIO4可以改写为IO3(OH)1,非羟基氧原子数目为3;
HClO中非羟基氧原子数目最少,酸性最弱,
故选A.
点评 本题考查了酸性强弱比较,根据含氧酸可用通式XOm(OH)n来表示,式中m大于等于2的是强酸,m为0的是弱酸,非羟基氧原子数目越大,酸性越强进行判断,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4. 按要求回答下列各题:
按要求回答下列各题:
(1)现有六种物质:①干冰;②金刚石;③四氯化碳;④氯化钙;⑤二氧化硅;⑥硫酸镁.请用编号填写下列空白:
(Ⅰ)熔化时需要破坏共价键的化合物是⑤
(Ⅱ)属于分子晶体且分子空间构型为直线型的是①,其电子式为
(Ⅲ)含有共价键的离子化合物是⑥.
(2)短周期中金属性最强的元素是Na(填元素符号);画出周期表中第三周期第VA族元素原子的结构示意图 ;第三周期元素中,形成简单离子半径最小的是Al3+(填离子符号)
;第三周期元素中,形成简单离子半径最小的是Al3+(填离子符号)
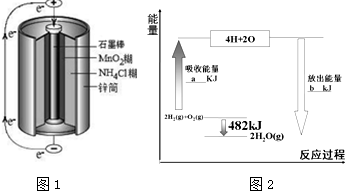
(3)锌锰干电池是最早使用的化学电源,其基本构造如图1所示.该电池的负极材料是Zn,若电路中通过0.4mole-,负极质量减少13g.工作时NH4+在正极放电产生两种气体,其中一种气体分子含10e-的微粒,正极的电极反应式为2NH4++2e-═2NH3↑+H2↑.
(4)拆开1mol气态物质中某种共价键需要吸收的能量,就是该共价键的键能.下表是某些共价键的键能:
根据图2中能量变化图,回答下列问题:
①图中:a=1370. ②表格中:X=463.
 按要求回答下列各题:
按要求回答下列各题:(1)现有六种物质:①干冰;②金刚石;③四氯化碳;④氯化钙;⑤二氧化硅;⑥硫酸镁.请用编号填写下列空白:
(Ⅰ)熔化时需要破坏共价键的化合物是⑤
(Ⅱ)属于分子晶体且分子空间构型为直线型的是①,其电子式为

(Ⅲ)含有共价键的离子化合物是⑥.
(2)短周期中金属性最强的元素是Na(填元素符号);画出周期表中第三周期第VA族元素原子的结构示意图
 ;第三周期元素中,形成简单离子半径最小的是Al3+(填离子符号)
;第三周期元素中,形成简单离子半径最小的是Al3+(填离子符号)(3)锌锰干电池是最早使用的化学电源,其基本构造如图1所示.该电池的负极材料是Zn,若电路中通过0.4mole-,负极质量减少13g.工作时NH4+在正极放电产生两种气体,其中一种气体分子含10e-的微粒,正极的电极反应式为2NH4++2e-═2NH3↑+H2↑.
(4)拆开1mol气态物质中某种共价键需要吸收的能量,就是该共价键的键能.下表是某些共价键的键能:
| 共价键 | H-H | O=O | H-O |
| 键能/kJ•mol-1 | 436 | 498 | X |
①图中:a=1370. ②表格中:X=463.
5.2013年3月19日我国宣布研制出“全碳气凝胶”,其密度是0.16mg/cm3,成为已知的最轻固态材料.对这种物质的认识正确的是( )
| A. | 是碳元素的一种同素异形体 | B. | 是碳元素的一种同位素原子 | ||
| C. | 全部由12C组成 | D. | 能溶于水 |
2.下列有关电池的说法不正确的是( )
| A. | 锌锰干电池中,锌电极是负极 | |
| B. | 手机上用的锂离子电池属于二次电池 | |
| C. | 甲烷燃料电池可把化学能转化为电能 | |
| D. | 铜锌原电池工作时,电子沿外电路从铜电极流向锌电极 |
19.用NA代表阿伏加德罗常数,下列有关叙述正确的是( )
| A. | 1mol冰中含氢键数为4NA | |
| B. | 12 g金刚石中含有C-C键的个数为4NA | |
| C. | 6 g SiO2晶体中硅氧共价键数为0.2NA | |
| D. | 常温下,100mLmol/LNa2CO3溶液中阴离子总数大于0.1NA |
6.以下用于研究有机物的方法错误的是( )
| A. | 蒸馏用于分离液态有机混合物 | |
| B. | 燃烧法是研究有机物成分的一种有效方法 | |
| C. | 核磁共振氢谱通常用于分析有机物的相对分子质量 | |
| D. | 对有机物分子红外光谱图的研究有助于确定有机物分子中的基团 |
4.关于主族元素的叙述,不正确的是( )
| A. | 元素原子的最外层电子数等于主族族序数 | |
| B. | 元素的最高价等于原子最外层电子数 | |
| C. | 最低负价数的绝对值等于原子最外层变稳定结构时所需电子数 | |
| D. | 同周期元素原子具有相同的核外电子层数 |
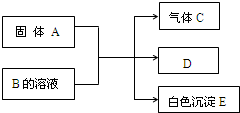 A、B、C、D、E均为中学化学的常见单质或化合物,它们之间的反应关系如图所示,其中A是短周期中原子半径最大的元素构成的单质,E既可溶于盐酸又可溶于NaOH溶液.
A、B、C、D、E均为中学化学的常见单质或化合物,它们之间的反应关系如图所示,其中A是短周期中原子半径最大的元素构成的单质,E既可溶于盐酸又可溶于NaOH溶液. .
.