题目内容
5.2013年3月19日我国宣布研制出“全碳气凝胶”,其密度是0.16mg/cm3,成为已知的最轻固态材料.对这种物质的认识正确的是( )| A. | 是碳元素的一种同素异形体 | B. | 是碳元素的一种同位素原子 | ||
| C. | 全部由12C组成 | D. | 能溶于水 |
分析 根据题中信息可知,“全碳气凝胶”为碳元素的不同单质,属于碳元素的同素异形体,再结合碳元素的性质可知该物质应该不溶于水,据此进行判断.
解答 解:A.“全碳气凝胶”是0.16mg/cm3,成为已知的最轻固态材料,则该物质为碳元素的原则同素异形体,故A正确;
B.同位素研究的是原子之间关系,而“全碳气凝胶”是一种具体物质,所以一定不是同位素,故B错误;
C.题中信息无法判断组成该物质的碳原子核素类型,不一定为12C,故C错误;
D.碳元素的单质一般难溶于水,故D错误;
故选A.
点评 本题考查了同素异形体、同位素的判断,题目难度不大,明确同位素、同素异形体的概念为解答根据,试题侧重考查学生的分析、理解能力及知识迁移能力.

练习册系列答案
相关题目
15.标准状况下,将5.6L由CO、CH4、C2H4、C2H2组成的混合气体与18L O2置于某密闭容器中点燃,完全反应后恢复到初始状况,得7.5LCO2,则下列判断正确的是( )
| A. | 完全反应后不可能有O2剩余 | |
| B. | 原混合气体中C2H4与C2H2的体积共为1.9L | |
| C. | 完全反应后生成水的质量为9 g | |
| D. | 原混合气体中CO与CH4的体积之比一定为1:1 |
16.下列离子方程式中,正确的是( )
| A. | 向Ba(OH)2溶液中滴加NaHSO4溶液至恰好为中性:Ba2++OH-+H++SO42-=BaSO4↓+H2O | |
| B. | NH4HCO3溶液与过量KOH浓溶液共热:NH4++OH- $\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| C. | 稀硝酸和过量的铁屑反应:3 Fe+8H++2 NO3-=3 Fe3++2 NO↑+4 H2O | |
| D. | KI溶液与H2SO4酸化的H2O2溶液混合:2 I-+H2O2+2H+=2H2O+I2 |
13.下列电子式书写错误的是( )
| A. |  | B. | N??N | C. |  | D. | 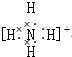 |
20.设NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A. | 0.1 mol H2O和D2O组成的混合物中含有中子数是NA | |
| B. | 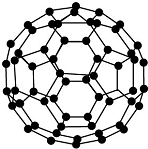 28 g N60(分子结构如图所示)中含有的N-N键数目为1.5NA | |
| C. | 0℃、1.01×105 Pa时,11.2 L氧气中所含的原子数约为NA | |
| D. | 常温下,将5.6 g铁投入足量的稀硫酸中,充分反应,转移电子数为0.3NA |
10.下列物质不属于大气污染物的是( )
| A. | CO | B. | N2 | C. | PM2.5 | D. | NxOy (氮氧化物) |
17.IIA族元素从第二周期到到第六周期的元素分别是Be(铍)、Mg(镁)、Ca(钙)、Sr(锶)、Ba(钡).下列关于ⅡA族元素预言可能正确的是( )
①常温下,单质铍能与水剧烈反应放出H2
②常温下,单质钡能与水剧烈反应放出H2
③Be(OH)2易溶于水
④Ba(OH)2易溶于水
⑤SrCO3易溶于水.
①常温下,单质铍能与水剧烈反应放出H2
②常温下,单质钡能与水剧烈反应放出H2
③Be(OH)2易溶于水
④Ba(OH)2易溶于水
⑤SrCO3易溶于水.
| A. | ①②③ | B. | ③⑤ | C. | ②④ | D. | ①②③④⑤ |
14.下列含氧酸中,酸性最弱的是( )
| A. | HClO | B. | HNO2 | C. | H2SO4 | D. | HIO4 |
 ,乙炔的电子式为
,乙炔的电子式为
 的名称是3,3,4-三甲基己烷;
的名称是3,3,4-三甲基己烷; CH2=CH-CO18OCH2CH3+H2O.
CH2=CH-CO18OCH2CH3+H2O.